Artículo dedicado a mis extraordinarios compañeros de Espacio Apnea - Formación OnLine:
Mónica González, Neumóloga José Ramón Alonso, Neurocientífico Emilio Macías, Ortodoncista
I. Introducción: La Doctrina de la Neurona como Piedra Angular de la Neurofisiología Respiratoria
La obra de Santiago Ramón y Cajal, galardonado con el Premio Nobel de Fisiología o Medicina en 1906 y padre indiscutible de la neurociencia, no es meramente un compendio de observaciones anatómicas; es la génesis de un paradigma. Su trabajo representa el marco conceptual sin el cual la comprensión contemporánea del sistema nervioso, y por extensión de la neurofisiología respiratoria, sería inconcebible. Cajal no solo describió la morfología de las células nerviosas con una precisión artística y científica sin precedentes; poseía lo que se ha descrito como un “extraordinario sentido de las implicaciones funcionales de su trabajo”. Esta capacidad casi profética para deducir la función a partir de la forma le permitió establecer los principios fundamentales que hoy sustentan desde la investigación básica del ritmo respiratorio hasta el tratamiento de patologías complejas como la apnea del sueño y la insuficiencia ventilatoria en enfermedades neuromusculares.
El pilar de su legado es la Doctrina de la Neurona. Antes de Cajal, la visión predominante era la teoría reticular, defendida por su contemporáneo y co-receptor del Nobel, Camillo Golgi, que postulaba el sistema nervioso como un sincitio: una red continua e ininterrumpida de protoplasma. Utilizando y perfeccionando la misma técnica de tinción con nitrato de plata desarrollada por Golgi, Cajal demostró de manera irrefutable lo contrario: el sistema nervioso está compuesto por miles de millones de células individuales, las neuronas, que son entidades anatómica y funcionalmente discretas. Estas células, aunque no se tocan, se comunican entre sí de manera altamente específica en puntos de contacto especializados, que más tarde Charles Sherrington denominaría sinapsis. Esta concepción, hoy elemental, constituyó una revolución copernicana en la biología y sentó las bases de toda la neurociencia posterior.
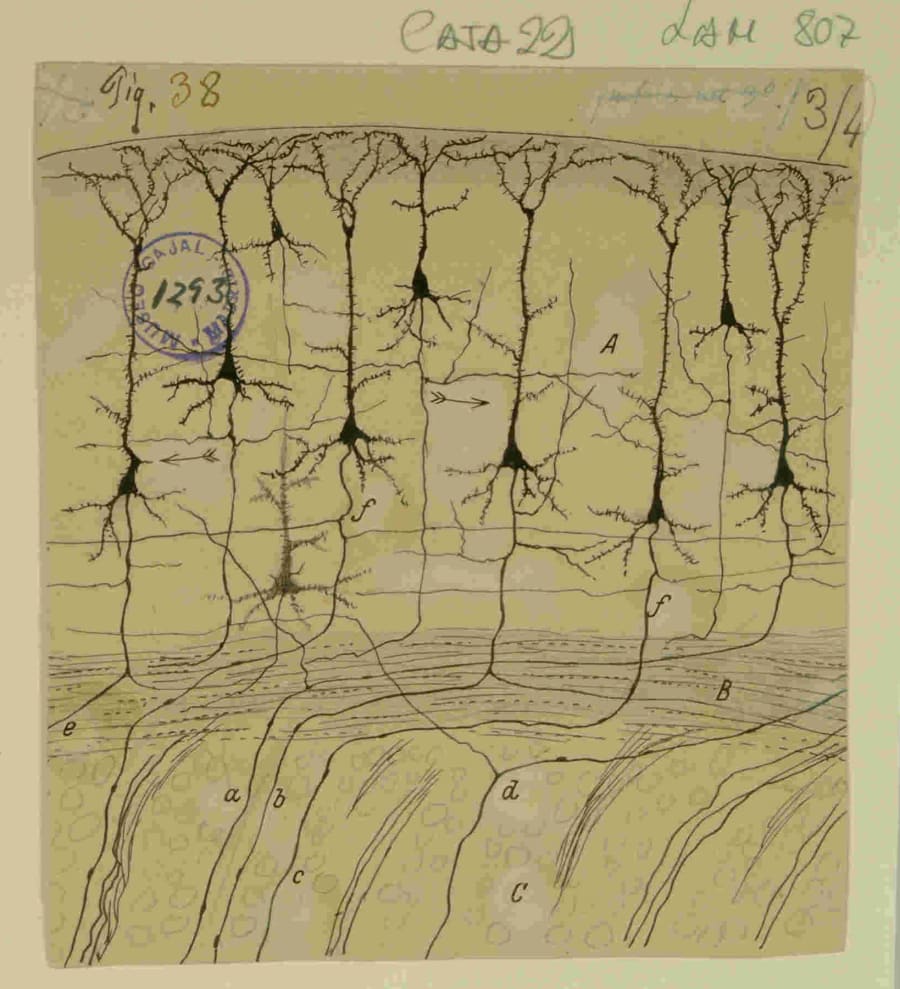
Existe un linaje intelectual directo y rastreable que conecta el microscopio de Cajal en el siglo XIX con los sofisticados laboratorios de sueño y las unidades de cuidados intensivos del siglo XXI. La comprensión de cómo una red neuronal en el tronco del encéfalo puede fallar durante un evento apnéico, o cómo la degeneración de motoneuronas específicas conduce a la parálisis del diafragma, es fundamentalmente dependiente de la premisa cajaliana. Sin la Doctrina de la Neurona, sería imposible conceptualizar la existencia de poblaciones neuronales especializadas, como las que generan el ritmo respiratorio, o de vías motoras específicas, cuya disfunción selectiva da lugar a patologías concretas.
La trascendencia de la Doctrina de la Neurona va más allá de la mera descripción estructural; es el fundamento de la especificidad funcional en el sistema nervioso. Si el cerebro fuera el retículo continuo que Golgi imaginaba, sería extremadamente difícil explicar cómo un pequeño y localizado grupo de neuronas en el bulbo raquídeo puede ser el principal responsable de generar el ritmo vital de la respiración, mientras que las neuronas adyacentes participan en funciones completamente distintas. La doctrina de Cajal permite la existencia de “centros” y “circuitos” especializados, un concepto que es la base de la neuroanatomía funcional.
Esta victoria conceptual sobre el reticularismo tiene implicaciones clínicas de una profundidad inmensa. Al establecer que el sistema nervioso está compuesto por unidades discretas que forman vías específicas, Cajal lo definió implícitamente como un sistema direccionable. Debido a que las neuronas son elementos individuales que construyen circuitos definidos, pueden ser el objetivo de intervenciones terapéuticas. El éxito de terapias modernas como la estimulación cerebral profunda o, de manera más pertinente para este análisis, la estimulación del nervio hipogloso para la apnea del sueño, es una consecuencia directa de este principio. Es posible modular una función específica porque se puede acceder y estimular las células y vías concretas responsables de ella. Este enfoque sería conceptualmente absurdo en un marco reticular, donde cualquier estimulación se disiparía difusamente a través de la red continua. Por lo tanto, la existencia misma de estas neuroterapias avanzadas no solo valida el modelo de Cajal, sino que demuestra el poder práctico y clínico de la Doctrina de la Neurona. Cada vez que un dispositivo restaura la respiración de un paciente estimulando un nervio específico, se rinde un homenaje implícito a la visión fundamental de Santiago Ramón y Cajal.
II. La Arquitectura del Control Respiratorio: Una Red Cajaliana en el Tronco Encefálico
El control automático de la respiración, ese metrónomo silencioso que marca el ritmo de nuestra existencia incluso en el sueño profundo o la inconsciencia, es orquestado por una intrincada red de neuronas en el tronco del encéfalo. Esta red es un ejemplo paradigmático de un circuito cajaliano: un conjunto de poblaciones neuronales distintas, interconectadas de manera precisa, cuya actividad coordinada da lugar a una función fisiológica compleja y rítmica. La organización de este sistema, desde sus generadores de ritmo centrales hasta sus vías de salida motoras, refleja los principios de especificidad celular y polarización dinámica que Cajal defendió con tanto ahínco.
El Centro de Control Central
El centro respiratorio se localiza bilateralmente en el bulbo raquídeo y la protuberancia (o puente de Varolio). No es una estructura monolítica, sino un sistema distribuido compuesto por varios grupos neuronales funcionalmente distintos pero interconectados:
-
El Grupo Respiratorio Dorsal (GRD): Ubicado principalmente en el núcleo del tracto solitario, este grupo está compuesto en su mayoría por neuronas inspiratorias. Recibe información sensorial crucial de quimiorceptores periféricos y mecanorreceptores pulmonares, desempeñando un papel clave en la modulación refleja del ritmo respiratorio básico.
-
El Grupo Respiratorio Ventral (GRV): Es una columna de neuronas más extensa que contiene tanto neuronas inspiratorias como espiratorias. Durante la respiración tranquila, permanece relativamente inactivo, pero se vuelve fundamental durante el ejercicio o cuando se requiere una ventilación forzada, proporcionando el impulso motor adicional a los músculos respiratorios accesorios.
-
El Grupo Respiratorio Pontino: Localizado en la protuberancia, este grupo, que incluye el centro apnéustico y el centro neumotáxico, no genera el ritmo primario, sino que lo modula, afinando la transición entre la inspiración y la espiración y asegurando un patrón respiratorio suave y regular.
Este sistema opera de manera predominantemente automática, bajo el control del sistema nervioso autónomo. Sin embargo, la respiración es única en el sentido de que también puede ser sometida a un control voluntario. Este control se origina en la corteza cerebral y desciende a través de los tractos corticoespinales para actuar directamente sobre las motoneuronas respiratorias, permitiéndonos contener la respiración, hablar o cantar. Esta doble vía de control, una automática y otra voluntaria, ilustra la organización jerárquica del sistema nervioso, donde los centros superiores pueden anular temporalmente los patrones rítmicos generados en el tronco encefálico.
El Complejo pre-Bötzinger: El “Noeud Vital” de la Respiración
Dentro del Grupo Respiratorio Ventral yace una subregión de importancia capital: el complejo pre-Bötzinger (preBötC). Descubierto en 1991 por Jack Feldman y sus colaboradores, este pequeño núcleo bilateral de interneuronas en el bulbo ventrolateral es ahora universalmente reconocido como el núcleo generador del ritmo inspiratorio. Su identificación representó la localización anatómica del “nudo vital” (noeud vital), el punto esencial para la respiración que el fisiólogo francés Pierre Flourens había postulado en el siglo XIX mediante estudios de lesión.
El preBötC es la personificación de un generador de patrones central. Contiene un núcleo de neuronas excitatorias, principalmente glutamatérgicas, que poseen propiedades intrínsecas de marcapasos y forman una red recurrente que les permite generar una actividad rítmica y sincronizada. Este ritmo inspiratorio primordial es luego transmitido a las neuronas premotoras y, finalmente, a las motoneuronas que inervan los músculos respiratorios, como las del nervio frénico (para el diafragma) y las del nervio hipogloso (para la lengua). Este flujo de información, desde el generador de ritmo hasta los efectores motores, es una demostración perfecta del principio de polarización dinámica de Cajal, que postula que el impulso nervioso viaja en una dirección predecible y unidireccional a través de la neurona, desde las dendritas hacia el axón.
La función del preBötC no se limita a generar un ritmo monótono. La red es altamente plástica, sujeta a la modulación por una vasta gama de neurotransmisores (como la serotonina, la noradrenalina y los opioides) y neuropéptidos (como la sustancia P). Esta neuromodulación permite que el mismo circuito reconfigure su patrón de salida para producir no solo la respiración normal (eupnea), sino también variantes conductuales como los suspiros o los jadeos. Esta capacidad de reconfiguración dota al sistema respiratorio de la flexibilidad necesaria para adaptarse a las cambiantes demandas metabólicas y conductuales del organismo.
La obra de Cajal, aunque anterior al descubrimiento del preBötC, fue notablemente profética. En sus meticulosos estudios sobre las vías centrales de los nervios craneales, describió con gran detalle las terminaciones de las fibras aferentes de los nervios vago y glosofaríngeo en el núcleo del tracto solitario (NTS). Hoy sabemos que estas son precisamente las vías a través de las cuales la información de los quimiorceptores periféricos (que detectan los niveles de O2 y CO2 en la sangre) y los mecanorreceptores pulmonares llega al tronco encefálico. El NTS, a su vez, proyecta e influye directamente en la actividad del preBötC y otros núcleos respiratorios. Por lo tanto, al cartografiar con precisión el “lado de entrada” del circuito de control respiratorio, Cajal sentó las bases anatómicas para la comprensión moderna del arco reflejo quimiosensorial. Sus “consideraciones funcionales proféticas” no fueron meras especulaciones, sino deducciones lógicas basadas en la exquisita organización estructural que observó, un testimonio de su capacidad única para vincular la forma con la función.
El Eslabón de la Escuela de Cajal: Fernando de Castro y los Sensores de la Respiración
Si bien Cajal cartografió las estructuras centrales, fue uno de sus discípulos más brillantes, Fernando de Castro (1896-1967), quien desveló un componente periférico esencial del control respiratorio. Aplicando con maestría las técnicas histológicas heredadas de su maestro, De Castro se centró en el estudio de la región carotídea. En una serie de trabajos fundamentales publicados entre 1926 y 1928, demostró que el cuerpo carotídeo (o glomus caroticum) no era una glándula, como se creía, sino un órgano sensorial con una rica inervación.
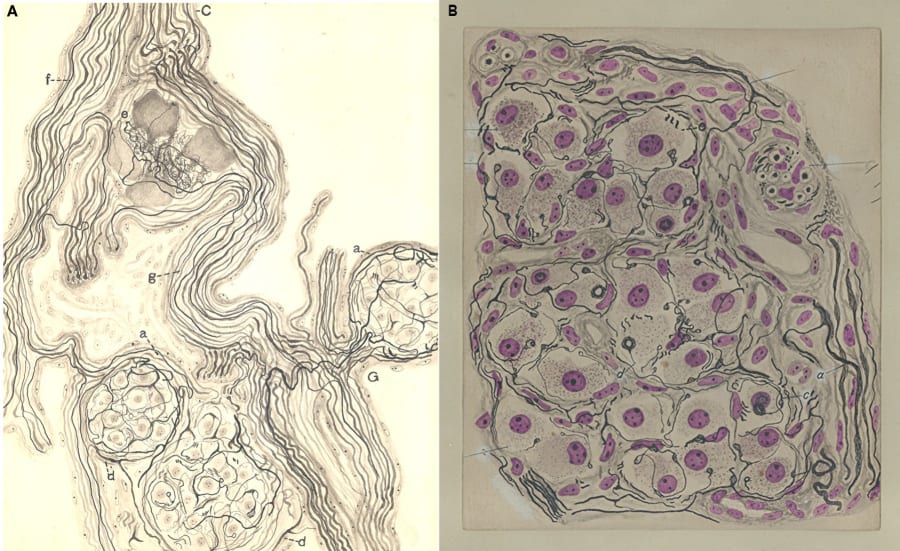
De Castro fue el primero en describir anatómicamente esta estructura como un conjunto de quimiorreceptores, diseñados para detectar cambios en la composición química de la sangre (como los niveles de oxígeno y dióxido de carbono). Crucialmente, los distinguió de los barorreceptores (sensores de presión) que Heinrich Hering había descrito en el seno carotídeo adyacente. Este descubrimiento proporcionó la base anatomofuncional para entender los reflejos cardiorrespiratorios que regulan la ventilación. La hipótesis anatómica de De Castro fue posteriormente confirmada fisiológicamente por el científico belga Corneille Heymans, quien, por esta demostración, recibió el Premio Nobel de Fisiología o Medicina en 1938. A pesar de que el propio comité del Nobel reconoció el trabajo de De Castro como fundamental, el científico español nunca fue nominado, en parte debido al trágico aislamiento de España durante la Guerra Civil. El trabajo de Fernando de Castro representa, por tanto, un puente indispensable entre la neuroanatomía de Cajal y la fisiología respiratoria moderna.
III. La Vía Final Común: El Control Neuromuscular de la Respiración
Una vez que el ritmo respiratorio es generado y modulado en el tronco encefálico, debe ser traducido en una acción mecánica coordinada. Esta tarea recae en la “vía final común” de Sherrington: las motoneuronas que inervan los músculos respiratorios. El acto de respirar no es una simple contracción muscular, sino una sinfonía neuromuscular exquisitamente temporizada que involucra dos sistemas motores distintos pero sincronizados: un sistema espinal que controla la “bomba” ventilatoria y un sistema craneal que asegura la permeabilidad de la “válvula” de la vía aérea superior. La integridad y coordinación de ambos son esenciales para una respiración eficaz, y su disfunción selectiva subyace a patologías respiratorias devastadoras.
La Bomba Ventilatoria: El Diafragma y los Músculos Intercostales
La principal fuerza motriz de la inspiración es la contracción del diafragma, un músculo en forma de cúpula inervado por las motoneuronas del nervio frénico, cuyos cuerpos celulares se encuentran en la médula espinal cervical, entre los niveles C3 y C5. El impulso rítmico inspiratorio generado en el bulbo raquídeo desciende a través de los tractos bulboespinales para activar sincrónicamente estas motoneuronas frénicas. Su activación provoca que el diafragma se aplane y descienda, aumentando el volumen de la cavidad torácica y generando la presión negativa que atrae el aire hacia los pulmones.
Durante la respiración tranquila, la espiración es un proceso mayormente pasivo, impulsado por el retroceso elástico de los pulmones y la pared torácica una vez que el diafragma se relaja. Sin embargo, durante estados de alta demanda ventilatoria, como el ejercicio, o en maniobras como la tos, la espiración se vuelve activa. Esto requiere el reclutamiento de músculos espiratorios, principalmente los músculos abdominales y los intercostales internos, controlados por motoneuronas de la médula espinal torácica y lumbar. La activación de estos músculos se produce por la inhibición de las motoneuronas inspiratorias y la excitación de las motoneuronas espiratorias, en un patrón de inervación recíproca orquestado por el centro respiratorio central.
La Permeabilidad de la Vía Aérea Superior: El Papel de los Nervios Craneales
La vía aérea superior (VAS), que comprende la faringe y la laringe, no es un conducto rígido, sino un tubo colapsable rodeado por más de 20 pares de músculos dilatadores y constrictores. Mantener su permeabilidad, especialmente durante la inspiración, es una tarea neuromuscular activa y crítica. Esta función está mediada por un conjunto de nervios craneales que se originan en el tronco encefálico, entre los que destacan:
-
El nervio hipogloso (par craneal XII): Inerva los músculos de la lengua, incluido el geniogloso, que es el principal músculo protusor de la lengua y un dilatador faríngeo clave.
-
El nervio glosofaríngeo (par craneal IX): Proporciona inervación motora a músculos como el estilofaríngeo, que eleva y ensancha la faringe.
-
El nervio vago (par craneal X): A través de sus ramas faríngeas y laríngeas, controla los músculos constrictores de la faringe y los músculos intrínsecos de la laringe, que regulan la apertura de la glotis.
Para que la respiración sea efectiva, la activación de estos músculos de la VAS debe estar perfectamente sincronizada con la de la bomba ventilatoria. De hecho, la actividad de los músculos dilatadores faríngeos, como el geniogloso, precede en milisegundos a la contracción del diafragma en cada ciclo inspiratorio. Esta activación anticipatoria, impulsada por el generador central del ritmo, tiene un propósito fundamental: rigidizar las paredes de la faringe para que puedan resistir la presión negativa generada por el diafragma y evitar así el colapso inspiratorio. La respiración, por lo tanto, es el resultado de la coexistencia y perfecta armonización de estos dos sistemas motores, el espinal y el craneal.
Esta delicada coordinación es profundamente dependiente del estado de conciencia. Durante la vigilia, un nivel tónico de actividad en los músculos de la VAS ayuda a mantener la faringe permeable. Sin embargo, durante el sueño, este control cambia drásticamente. A medida que se profundiza el sueño, se produce una progresiva relajación muscular que culmina en la fase de movimientos oculares rápidos (sueño REM), cuya característica definitoria es una atonía muscular generalizada mediada centralmente. Este proceso fisiológico, que nos impide representar físicamente nuestros sueños, implica una potente inhibición de la mayoría de las motoneuronas esqueléticas.
El diafragma, crucial para la supervivencia, está en gran medida exento de esta atonía REM, permitiendo que la respiración continúe. Sin embargo, los músculos dilatadores de la VAS no gozan de la misma protección. Su actividad tónica y fásica disminuye drásticamente, lo que reduce la rigidez de la vía aérea y la vuelve sumamente vulnerable al colapso. Este fenómeno fisiológico normal es la clave para entender la patogénesis de la apnea obstructiva del sueño (AOS). La AOS no surge de un mecanismo patológico de novo, sino de la interacción de una anatomía predisponente (por ejemplo, una mandíbula pequeña, amígdalas grandes o depósitos de grasa en el cuello) con la inhibición neuromuscular fisiológica y normal del sueño REM. La enfermedad es, en esencia, una propiedad emergente de esta interacción entre una estructura vulnerable y un estado de control neuronal alterado pero fisiológico.
IV. Fisiopatología del Control Respiratorio: Cuando la Red Neuronal Falla
La robustez del sistema de control respiratorio es notable, pero no infalible. Diversas patologías pueden perturbar su funcionamiento en distintos niveles de la jerarquía de control, desde el generador central del ritmo hasta las motoneuronas efectoras. Estas disfunciones dan lugar a un espectro de trastornos respiratorios, cada uno con una firma fisiopatológica única que refleja el punto de fallo específico dentro de la red neuronal. La apnea obstructiva del sueño (AOS), la apnea central del sueño y la insuficiencia respiratoria en enfermedades neuromusculares (ENM) representan arquetipos de fallo en el control motor periférico, la generación del ritmo central y la integridad de la vía motora, respectivamente.
Tabla 1: Comparativa Fisiopatológica de los Trastornos Respiratorios del Sueño y Neuromusculares
TrastornoNivel Primario de Disfunción NeuronalMecanismo Fisiopatológico PrincipalManifestación Clínica PrimariaApnea Obstructiva del Sueño (AOS)Motoneuronas craneales de la vía aérea superior (hipogloso, vago)Inhibición fisiológica de la actividad muscular durante el sueño (especialmente REM) en una vía aérea anatómicamente susceptibleColapso faríngeo recurrente con esfuerzo respiratorio mantenido o aumentadoApnea Central del SueñoRed generadora del ritmo (Complejo pre-Bötzinger) y sus moduladoresCese transitorio del impulso respiratorio central; inestabilidad del control quimiorreflejo (ganancia de bucle elevada)Cese del esfuerzo respiratorio y del flujo aéreo**Insuficiencia Respiratoria en ENM (ej. ELA)**Motoneuronas espinales (frénicas, intercostales) y bulbares (craneales)Degeneración progresiva y muerte de las motoneuronasHipoventilación global (debilidad inspiratoria) y tos ineficaz (debilidad espiratoria)
El Colapso de la Vía Aérea: Apnea Obstructiva del Sueño (AOS)
La AOS es el trastorno respiratorio del sueño más prevalente y se caracteriza por episodios repetidos de obstrucción parcial (hipopnea) o completa (apnea) de la vía aérea superior durante el sueño, a pesar del esfuerzo respiratorio continuo. Como se ha esbozado, su fisiopatología es un mosaico multifactorial, resultado de una compleja interacción entre factores anatómicos y funcionales (neuromusculares). Esta intrincada red de factores subraya la necesidad de una formación especializada y colaborativa, un pilar fundamental del Abordaje Multidisciplinar en el Diagnóstico y Tratamiento de la Apnea Obstructiva del Sueño (AOS).
Anatómicamente, los pacientes con AOS a menudo presentan una vía aérea superior más estrecha o “congestionada” debido a características como la retrognatia (mandíbula retraída), macroglosia (lengua grande), hipertrofia amigdalar o depósitos de grasa en las paredes faríngeas laterales, un factor de riesgo fuertemente asociado a la obesidad. Sin embargo, la anatomía por sí sola no explica la enfermedad. El componente funcional es igualmente crítico. Durante el sueño, la actividad de los músculos dilatadores de la faringe, como el geniogloso, disminuye fisiológicamente. En individuos con una VAS ya comprometida, esta pérdida de tono muscular, que alcanza su nadir durante la atonía del sueño REM, es suficiente para permitir que la presión inspiratoria negativa generada por el diafragma succione y colapse las paredes faríngeas.
Además de este mecanismo central, otros factores neurofisiológicos contribuyen a la perpetuación y gravedad de la AOS:
-
Umbral de despertar bajo: Algunos pacientes se despiertan con perturbaciones respiratorias muy leves. Aunque el despertar restaura el tono muscular y abre la vía aérea, también fragmenta el sueño, impidiendo alcanzar las fases más profundas y reparadoras.
-
Ganancia de bucle elevada (High Loop Gain): Se refiere a una respuesta ventilatoria excesivamente sensible y vigorosa a los cambios en los gases sanguíneos. Tras una apnea, la acumulación de CO2 y la caída de O2 desencadenan una hiperventilación desproporcionada. Esta sobrerreacción reduce rápidamente el CO2 por debajo del umbral apneico, lo que a su vez provoca una apnea central o facilita un nuevo colapso obstructivo, creando un ciclo de inestabilidad.
Las consecuencias sistémicas de la AOS son graves. Los ciclos recurrentes de hipoxia y reoxigenación, junto con la fragmentación del sueño y los despertares asociados a ráfagas de actividad del sistema nervioso simpático, generan estrés oxidativo, inflamación y disfunción endotelial. Estos mecanismos son los principales responsables de la alta prevalencia de comorbilidades cardiovasculares en pacientes con AOS, como la hipertensión arterial, la fibrilación auricular, la insuficiencia cardíaca y un mayor riesgo de accidente cerebrovascular. La solidez de esta conexión y la eficacia del tratamiento han sido confirmadas de manera contundente por un reciente y masivo estudio publicado en el prestigioso European Respiratory Journal, en el que han participado centros españoles de referencia como la Unidad de Sueño y Ventilación del Hospital Marqués de Valdecilla, liderada por la Dra. Mónica González. Tras seguir a más de 5.000 pacientes durante 14 años, los resultados son inequívocos: la terapia con presión positiva continua en la vía aérea (CPAP) reduce en un 16% el riesgo de eventos cardiovasculares mayores y mortalidad. Este estudio no solo valida científicamente la CPAP como una de las terapias domiciliarias más coste-efectivas del arsenal terapéutico actual, sino que también ha permitido desarrollar una innovadora calculadora de riesgo que promete revolucionar la toma de decisiones clínicas, un avance que subraya la importancia de la medicina basada en la evidencia.
Más allá de las consecuencias cardiovasculares, la fragmentación del sueño inherente a la AOS ataca un mecanismo de mantenimiento neurológico fundamental: el sistema glinfático. Descubierto recientemente, este sistema funciona como un servicio de limpieza cerebral, eliminando desechos metabólicos como la proteína beta-amiloide, cuya acumulación se asocia con la enfermedad de Alzheimer. Este proceso de depuración es más activo durante el sueño profundo de ondas lentas, precisamente la fase que los pacientes con AOS rara vez alcanzan de forma sostenida debido a los microdespertares constantes. La interrupción de esta limpieza nocturna proporciona un vínculo neurobiológico directo entre la AOS y el deterioro cognitivo, explicando síntomas como la pérdida de memoria y la dificultad de concentración. A largo plazo, esta disfunción glinfática podría posicionar a la AOS como un factor de riesgo significativo para el desarrollo de enfermedades neurodegenerativas, añadiendo una nueva dimensión de urgencia a su diagnóstico y tratamiento temprano.
El Silencio Central: Apnea Central del Sueño
A diferencia de la AOS, en la apnea central del sueño (ACS) el problema no es una obstrucción mecánica, sino un fallo en el origen del impulso respiratorio. El cerebro, específicamente el centro respiratorio del tronco encefálico, deja de enviar transitoriamente las señales necesarias a los músculos respiratorios. El resultado es el cese tanto del esfuerzo respiratorio como del flujo aéreo.
La ACS puede ser causada por diversas condiciones que afectan la capacidad del tronco encefálico para controlar la respiración:
-
Insuficiencia Cardíaca Congestiva: Es la causa más común de un tipo específico de ACS conocido como respiración de Cheyne-Stokes. La circulación sanguínea enlentecida retrasa la llegada de la información de los quimiorceptores al cerebro, lo que, combinado con una ganancia de bucle elevada, genera un patrón cíclico de hiperpnea creciente (crescendo) y apnea decreciente (decrescendo).
-
Lesiones del Tronco Encefálico: Un accidente cerebrovascular, un tumor o un traumatismo que afecte directamente al bulbo raquídeo o la protuberancia puede dañar las neuronas del centro respiratorio, incluido el complejo preBötC.
-
Fármacos: Los medicamentos depresores del sistema nervioso central, en particular los opioides (morfina, oxicodona), son potentes supresores de la actividad del preBötC y pueden inducir ACS o respiración irregular.
-
Apnea Central Idiopática: En raras ocasiones, no se puede identificar una causa subyacente, y el trastorno se considera primario.
La Degeneración de la Unidad Motora: Insuficiencia Respiratoria en Enfermedades Neuromusculares (ENM)
En las ENM, el fallo respiratorio no se debe a un colapso intermitente ni a un fallo del generador central, sino a la destrucción progresiva e inexorable de la propia vía motora. La Esclerosis Lateral Amiotrófica (ELA), también conocida como enfermedad de Lou Gehrig, representa el arquetipo más desolador de esta condición. La ELA se caracteriza por la muerte de las motoneuronas superiores (en la corteza cerebral) e inferiores (en el tronco encefálico y la médula espinal). A medida que estas neuronas degeneran, los músculos que inervan se debilitan, se atrofian y finalmente se paralizan.
Cuando este proceso afecta a los músculos respiratorios, surgen dos consecuencias fatales que definen la insuficiencia respiratoria neuromuscular:
-
Debilidad de los Músculos Inspiratorios: La debilidad progresiva del diafragma y los intercostales externos reduce la capacidad de generar un volumen corriente adecuado. Esto conduce a una hipoventilación alveolar crónica. Inicialmente, esta hipoventilación es más evidente durante el sueño, especialmente en la fase REM, cuando el tono de los músculos posturales y accesorios disminuye y la carga recae casi exclusivamente en un diafragma debilitado. Con el tiempo, la hipoventilación se manifiesta también durante el día, provocando una retención crónica de CO2 (hipercapnia) y una disminución de O2 (hipoxemia).
-
Debilidad de los Músculos Espiratorios: La parálisis de los músculos abdominales y los intercostales internos incapacita al paciente para generar las altas presiones intratorácicas necesarias para una tos efectiva. Una tos ineficaz impide la correcta eliminación de secreciones de la vía aérea. Esto conduce a la retención de secreciones, atelectasias (colapso de alvéolos) y, de manera crítica, a neumonías recurrentes por aspiración, que son una causa principal de hospitalización y mortalidad.
La progresión es implacable. La insuficiencia respiratoria, ya sea por fallo ventilatorio crónico o por una complicación infecciosa aguda debida a la tos ineficaz, es la causa más común de muerte en pacientes con ELA.
Es importante reconocer que, aunque estos tres trastornos representan arquetipos de fallo en distintos niveles del sistema, en la práctica clínica sus mecanismos pueden solaparse. Un paciente con ENM y debilidad de los músculos faríngeos puede desarrollar un componente obstructivo superpuesto a su hipoventilación restrictiva. De manera similar, un paciente con AOS grave y de larga evolución puede desarrollar hipercapnia crónica, lo que a su vez puede desensibilizar los quimiorceptores centrales e introducir un componente de hipoventilación central. Esta superposición refleja la naturaleza profundamente integrada de la red de control respiratorio, donde el fallo en un componente puede desencadenar una cascada de perturbaciones en todo el sistema, un concepto que se alinea con una visión de la enfermedad desde la biología de sistemas.
V. La Vanguardia de la Formación: Abordaje Multidisciplinar de la AOS
La complejidad de la Apnea Obstructiva del Sueño, con sus raíces tanto anatómicas como neurofisiológicas, exige un enfoque diagnóstico y terapéutico que trascienda las fronteras de una única especialidad. Reconocer y dominar esta complejidad es lo que distingue al profesional de vanguardia.
Para responder a esta necesidad crítica, Espacio APNEA y la Fundación General de la Universidad de Salamanca presentan la V Edición del curso “Abordaje Multidisciplinar en el Diagnóstico y Tratamiento de la Apnea Obstructiva del Sueño (AOS)”. Este programa de formación integral, que dará comienzo el 2 de marzo de 2026, está meticulosamente diseñado para profesionales de la salud que buscan no solo comprender, sino liderar en el campo de la medicina del sueño.
 V Edición del curso “Abordaje Multidisciplinar en el Diagnóstico y Tratamiento de la Apnea Obstructiva del Sueño (AOS)”
V Edición del curso “Abordaje Multidisciplinar en el Diagnóstico y Tratamiento de la Apnea Obstructiva del Sueño (AOS)”
Dirigido por un equipo de expertos que incluye la Dra. Mónica González, al Dr. José Ramón Alonso, el Dr. Emilio Macías y el farmacéutico José Francisco Adserias, el curso reúne a un claustro de ponentes de primer nivel. Entre ellos se encuentra la citada Dra. Mónica González, coautora del estudio histórico MACE or Death Risk in Obstructive Sleep Apnoea and the Effect of Positive Airway Pressure publicado en el European Respiratory Journal que ha demostrado de forma definitiva el impacto del tratamiento de la AOS en la reducción del riesgo cardiovascular. Esta es una oportunidad única para aprender directamente de los investigadores que están generando la evidencia que define la práctica clínica del futuro. El panel de expertos se completa con neurocientíficos, neumólogos, ortodoncistas, cirujanos maxilofaciales, odontólogos, neurofisiólogos, ORL y logopedas, garantizando una visión de 360 grados que refleja la realidad clínica diaria.
Con una estructura de 42 horas lectivas distribuidas en 6 módulos y 21 unidades docentes, el formato online permite una inmersión profunda en temas cruciales como la neurociencia del sueño, el diagnóstico de precisión (polisomnografía, poligrafía), el tratamiento con presión positiva, las intervenciones quirúrgicas, el uso de dispositivos intraorales y la terapia miofuncional. El aprendizaje se enriquece con 6 horas de tutorías en directo, material de vanguardia y la posibilidad de interactuar directamente con el profesorado.
¿Está listo para transformar su enfoque clínico y ofrecer las mejores soluciones a sus pacientes? Explore el programa completo y asegure su plaza en la V Edición aquí.
Este curso, avalado por sociedades de prestigio como la Sociedad Española de Neumología y Cirugía Torácica (SEPAR) y la Sociedad Española de Medicina Dental del Sueño (SEMDeS), es una inversión definitiva en su desarrollo profesional.
No deje pasar la oportunidad de aprender de los líderes en el campo. Inscríbase hoy y forme parte de la vanguardia en medicina del sueño.
VI. Intervenciones Terapéuticas Modernas: Restaurando el Ritmo y la Función
El conocimiento detallado de la neurofisiología respiratoria y de los puntos de fallo específicos en cada patología ha impulsado el desarrollo de un arsenal terapéutico cada vez más sofisticado. Las intervenciones modernas, como las destacadas en los programas de formación de Espacio APNEA, pueden ser reinterpretadas no como meros procedimientos médicos, sino como estrategias de ingeniería neuro-mecánica diseñadas para compensar, eludir o restaurar la función en puntos precisos del circuito cajaliano de la respiración.
Soporte a la Bomba Ventilatoria: Ventilación Mecánica No Invasiva (VMNI)
La VMNI es una terapia fundamental en el manejo de la insuficiencia respiratoria hipercápnica, especialmente en pacientes con ENM. Desde una perspectiva neurofisiológica, la VMNI actúa como un “diafragma externo”. Para los pacientes cuya musculatura inspiratoria está fallando debido a la muerte de las motoneuronas frénicas e intercostales, el ventilador proporciona el soporte de presión positiva necesario para inflar los pulmones, asegurar una ventilación alveolar adecuada y corregir la hipercapnia resultante.
El objetivo de la VMNI en la ENM es doble: por un lado, descarga y “descansa” los músculos respiratorios fatigados, rompiendo el círculo vicioso de debilidad y fallo ventilatorio; por otro, normaliza los gases sanguíneos, especialmente durante la noche, mejorando la calidad del sueño y los síntomas diurnos como la cefalea matutina y la somnolencia. El éxito de la terapia depende crucialmente de la correcta elección de los modos ventilatorios y los parámetros del ventilador para lograr una sincronía óptima entre el paciente y la máquina. Este desafío técnico consiste, en esencia, en acoplar un ritmo mecánico externo al ritmo neural residual y a las necesidades metabólicas del paciente.
Asistencia al Aclaramiento de Secreciones: Insuflación-Exsuflación Mecánica (MI-E)
Si la VMNI aborda el fallo de la bomba inspiratoria en la ENM, la Insuflación-Exsuflación Mecánica (MI-E), comúnmente conocida como “asistente de la tos” (Cough Assist), se dirige directamente al segundo fallo crítico: la debilidad de la bomba espiratoria y la consiguiente tos ineficaz.
El dispositivo MI-E simula una tos natural de manera mecánica. Primero, aplica una presión positiva para insuflar lentamente un gran volumen de aire en los pulmones, imitando una inspiración profunda. Inmediatamente después, cambia de forma abrupta a una presión negativa, succionando el aire rápidamente. Este cambio rápido de presión genera un flujo espiratorio máximo muy elevado, similar al de una tos vigorosa, que arrastra y moviliza las secreciones desde las vías aéreas periféricas hacia las centrales, desde donde pueden ser eliminadas. Neurofisiológicamente, la MI-E es un sustituto mecánico de la activación coordinada y de alta intensidad de las motoneuronas espiratorias abdominales e intercostales, una función que se ha perdido debido a la degeneración neuronal.
Reapertura de la Vía Aérea Superior en AOS
El tratamiento de la AOS se centra en prevenir el colapso faríngeo durante el sueño, y las estrategias para lograrlo abarcan desde la modificación biomecánica hasta la neuromodulación directa.
-
Intervenciones Biomecánicas: Los tratamientos odonto-estomatológicos, como los Dispositivos de Avance Mandibular (DAM) para adultos o las intervenciones de ortopedia dentofacial en niños, actúan modificando la estructura anatómica de la VAS. Un DAM, por ejemplo, posiciona la mandíbula y la lengua hacia adelante, aumentando el calibre de la vía aérea retrolingual y retrofaríngea. Estas terapias no corrigen la inhibición neuromuscular subyacente del sueño, sino que mejoran la estabilidad mecánica de la vía aérea de tal manera que la pérdida fisiológica de tono muscular ya no es suficiente para provocar su colapso. En efecto, reducen la demanda funcional sobre un sistema de control neuromuscular que se vuelve insuficiente durante el sueño.
-
Intervención Neuromodulatoria: Estimulación del Nervio Hipogloso (ENH): Esta terapia representa el enfoque más directo y elegante desde el punto de vista neurofisiológico para tratar la AOS. Es la aplicación clínica más pura de los principios cajalianos de especificidad y direccionabilidad neuronal. El sistema consta de tres componentes implantados: un sensor de presión en el espacio intercostal que detecta el esfuerzo inspiratorio, un generador de impulsos (similar a un marcapasos cardíaco) implantado en el pecho, y un electrodo de estimulación que se coloca alrededor del nervio hipogloso.
El funcionamiento es una obra de ingeniería biomédica sincronizada con la fisiología:
-
Al inicio de la inspiración, el sensor detecta el cambio de presión torácica.
-
Esta señal se transmite al generador de impulsos.
-
El generador envía un pulso eléctrico suave y sincronizado al electrodo que rodea el nervio hipogloso.
-
La estimulación del nervio hipogloso provoca la contracción del músculo geniogloso y otros músculos de la lengua, proyectándola hacia adelante.
-
Este movimiento anterior de la base de la lengua abre y estabiliza la vía aérea faríngea precisamente en el momento en que es más vulnerable al colapso: durante la inspiración.
La ENH no es una estimulación continua; es una neuromodulación fásica y sincronizada con la respiración que restaura artificialmente la actividad neuromuscular que se pierde fisiológicamente durante el sueño. Es, en efecto, un “marcapasos para la lengua”, que actúa directamente sobre una vía neural específica para corregir una disfunción compleja.
La evolución de estas terapias refleja un progreso en nuestra comprensión, desde la anatomía macroscópica hasta la neurofisiología de redes. Las primeras cirugías para la AOS, como la uvulopalatofaringoplastia, eran enfoques puramente anatómicos de resección de tejido. La CPAP actúa como una férula neumática, un soporte mecánico. La VMNI y la MI-E son bombas mecánicas que sustituyen la función muscular. La ENH, sin embargo, representa un cambio de paradigma. Es una terapia genuinamente neurofisiológica que interactúa directamente con una vía específica dentro del marco conceptual que Cajal nos legó. Su éxito es la prueba clínica definitiva de la Doctrina de la Neurona, tratando un nervio individual como un objetivo direccionable para restaurar una función vital. Este avance marca el camino hacia una medicina más personalizada, precisa y fundamentada en los principios de la neurociencia.
VII. Síntesis y Direcciones Futuras: De la Neurona a la Medicina de Sistemas
El recorrido desde los meticulosos dibujos de Santiago Ramón y Cajal hasta las complejas intervenciones en la medicina respiratoria moderna traza un arco intelectual de más de un siglo. Este viaje comienza con el establecimiento de la neurona como la unidad fundamental, discreta y funcional del sistema nervioso. Esta premisa fundamental permitió a generaciones posteriores de científicos concebir y demostrar cómo estas unidades individuales se ensamblan en circuitos funcionales con propiedades emergentes, como la capacidad del complejo pre-Bötzinger para generar un ritmo respiratorio autónomo. A su vez, la comprensión de estos circuitos generadores de patrones reveló cómo su actividad se propaga a través de vías motoras específicas para orquestar la compleja sinfonía neuromuscular de la respiración, un proceso que depende de la sincronización precisa entre efectores craneales y espinales.
Armados con este mapa funcional, hemos llegado a comprender las patologías respiratorias no como fallos sistémicos amorfos, sino como disfunciones localizables en puntos específicos de esta red. La apnea obstructiva del sueño se reveló como un fallo en la activación de las motoneuronas de la vía aérea superior durante el estado de inhibición del sueño; la apnea central, como un silencio en el propio generador del ritmo; y la insuficiencia respiratoria neuromuscular, como la desintegración de la vía motora final. Esta capacidad para diagnosticar el nivel del fallo ha sido la clave para desarrollar terapias cada vez más dirigidas, que han evolucionado desde el soporte mecánico general (VMNI) hasta la neuromodulación precisa y en tiempo real de vías neuronales específicas (ENH). Cada paso en este progreso ha sido una reafirmación del paradigma cajaliano: para entender y tratar el sistema, primero debemos entender sus componentes y cómo se conectan.
El Futuro: Hacia una Medicina de Redes Respiratorias
El legado de Cajal, sin embargo, no nos invita a la complacencia, sino que nos proporciona el lenguaje para formular las preguntas del futuro. La próxima frontera en la medicina respiratoria y la neurociencia se encuentra en la transición de un enfoque de circuito a un enfoque de medicina de sistemas o de redes. Las enfermedades como la AOS no son el resultado de un único gen defectuoso o una única molécula disfuncional. Son propiedades emergentes de un sistema dinámico y complejo en el que interactúan múltiples subsistemas: la anatomía craneofacial, el control neuromuscular, la sensibilidad de los quimiorreflejos (ganancia de bucle), el umbral de despertar y el estado metabólico general.
Desde esta perspectiva, el futuro del tratamiento no residirá únicamente en el desarrollo de mejores soluciones mecánicas o neuroprotésicas, sino en la capacidad de modular la estabilidad y la dinámica de toda la red de control respiratorio. La investigación ya está explorando esta vía. Por ejemplo, los ensayos farmacológicos que combinan atomoxetina (un inhibidor de la recaptación de noradrenalina) y oxibutinina (un antimuscarínico) buscan aumentar la actividad de las motoneuronas del hipogloso durante el sueño, un enfoque que intenta corregir la disfunción a nivel de neurotransmisores en lugar de eludirla con estimulación eléctrica. Otras investigaciones se centran en fármacos que puedan estabilizar el control respiratorio reduciendo la ganancia de bucle, como los inhibidores de la anhidrasa carbónica. Estos enfoques representan un intento de “recalibrar” la red en lugar de simplemente parchear sus salidas.
Santiago Ramón y Cajal, en una de sus reflexiones más célebres, afirmó que “Todo hombre puede ser, si se lo propone, escultor de su propio cerebro”. Esta declaración, que encapsula su creencia en la plasticidad neuronal y el poder de la voluntad, adquiere un nuevo significado en el siglo XXI. Al descifrar las intrincadas redes neuronales que él fue el primero en empezar a cartografiar, la ciencia y la medicina están aprendiendo a convertirse en escultoras de la función neuronal misma. El objetivo ya no es solo observar la belleza de la estructura, sino intervenir con precisión para restaurar la función, para devolver el ritmo vital de la vida, una respiración a la vez. En esta búsqueda, la fusión del humanismo científico de Cajal y las herramientas de la neurociencia continúan iluminando el camino, demostrando que la comprensión de los misterios más fundamentales de la biología es la ruta más segura hacia el alivio del sufrimiento humano.
VIII. Bibliografía
-
López-Muñoz, F., Boya, J., & Alamo, C. (2006). Neuron theory, the cornerstone of neuroscience, on the centenary of the Nobel Prize award to Santiago Ramón y Cajal. Brain Research Bulletin, 70(4-6), 391-405.
-
Ramón y Cajal, S. (1899-1904). Textura del sistema nervioso del hombre y de los vertebrados. Moya.
-
Smith, J. C., Ellenberger, H. H., Ballanyi, K., Richter, D. W., & Feldman, J. L. (1991). Pre-Bötzinger complex: a brainstem region that may generate respiratory rhythm in mammals. Science, 254(5032), 726-729.
-
Horner, R. L. (2008). Pathophysiology of obstructive sleep apnea. Journal of cardiopulmonary rehabilitation and prevention, 28(5), 289-298.
-
Divo, M. J., Martinez-Garcia, M. A., Gonzalez, M., Campos-Rodriguez, F., Lloberes, P., Marin-Oto, M., Forner, M., Sanz-Rubio, D., Nieto, D., Celli, B. R., & Marin, J. M. (2025). MACE or Death Risk in Obstructive Sleep Apnoea and the Effect of Positive Airway Pressure. European Respiratory Journal. Publicado en línea. https://doi.org/10.1183/13993003.00519-2025
-
Nedergaard, M., & Goldman, S. A. (2023, October 1). How Sleep Cleans the Brain and Keeps You Healthy. Scientific American.
-
Reddy, O. C., & van der Werf, Y. D. (2020). The Sleeping Brain: Harnessing the Power of the Glymphatic System through Lifestyle Choices. Brain sciences, 10(11), 868.
-
Benditt, J. O. (2009). Respiratory management of neuromuscular disease. European Respiratory Journal, 34(2), 444-451.
-
Strollo, P. J., Jr, Soose, R. J., Maurer, J. T., de Vries, N., Cornelius, J., Froymovich, O., Hanson, R. D., Padhya, T. A., Steward, D. L., Gillespie, M. B., Woodson, B. T., Van de Heyning, P. H., Goetting, M. G., Vanderveken, O. M., Feldman, N., Knaack, L., & Strohl, K. P. (2014). Upper-airway stimulation for obstructive sleep apnea. The New England journal of medicine, 370(2), 139–149.
-
McEvoy, R. D., Antic, N. A., Heeley, E., et al. (2016). CPAP for Prevention of Cardiovascular Events in Obstructive Sleep Apnea. The New England journal of medicine, 375(10), 919–931.
-
Agusti, A., Bel, E., Thomas, M., et al. (2018). The path to personalised medicine in respiratory diseases. European Respiratory Review, 27(147), 170110.
-
Yuste, R. (2015). From the neuron doctrine to neural networks. Nature Reviews Neuroscience, 16(8), 487-497.
-
de Castro, F. (2009). Towards the sensory nature of the carotid body: Hering, De Castro and Heymans. Frontiers in Neuroanatomy, 3, 23. https://doi.org/10.3389/neuro.05.023.2009
-
The Nobel Prize in Physiology or Medicine 1938. NobelPrize.org. Nobel Prize Outreach AB 2024. https://www.nobelprize.org/prizes/medicine/1938/heymans/facts/



Comentarios