Artículo dedicado al Dr. David Ezpeleta, Vicepresidente de la Sociedad Española de Neurología (SEN).
Contribuciones Fundacionales de Santiago Ramón y Cajal a la Comprensión de la Enfermedad de Alzheimer.
Resumen Ejecutivo
Análisis de las contribuciones seminales de Santiago Ramón y Cajal a la neurociencia de la demencia senil y, específicamente, de la enfermedad de Alzheimer. Aunque Alois Alzheimer fue quien describió la enfermedad, se argumenta que fue el trabajo fundamental de Cajal el que proporcionó el marco conceptual y biológico indispensable para comprender su patología.

El análisis se estructura en varias áreas clave. Primero, se establece cómo la Doctrina de la Neurona de Cajal, junto con sus principios de especificidad conexional y plasticidad, constituyó una revolución epistemológica que hizo posible el estudio de las enfermedades neurodegenerativas. Segundo, se examina su obra magna sobre la degeneración y regeneración del sistema nervioso, demostrando cómo sus descripciones de la “brotación abortiva” en el sistema nervioso central (SNC) predijeron los procesos celulares observados en el cerebro con Alzheimer. Tercero, se presenta evidencia directa, a través del redescubrimiento de sus preparaciones histológicas, de que Cajal estudió activamente la enfermedad, interpretando sus lesiones características a través de su propio y robusto marco mecanicista. Finalmente, se traza un linaje directo desde los conceptos de Cajal hasta las estrategias de investigación y terapéuticas del siglo XXI, demostrando que su legado no es meramente histórico, sino una influencia activa y persistente en la búsqueda de una cura. En conjunto, el artículo posiciona a Cajal no como un actor secundario, sino como el arquitecto intelectual invisible cuyo trabajo sentó las bases sobre las que se ha construido toda nuestra comprensión moderna de la enfermedad de Alzheimer.
Sección 1: El Marco Cajaliano: Estableciendo los Cimientos de la Neurociencia
Para comprender una enfermedad neurodegenerativa, primero es necesario disponer de una gramática fundamental del sistema nervioso. Santiago Ramón y Cajal no solo contribuyó a esta gramática, sino que fue el autor de sus capítulos más esenciales. Su Doctrina de la Neurona, sus principios de conectividad y sus incipientes ideas sobre la plasticidad no son meras notas a pie de página históricas, sino los prerrequisitos lógicos para todo el campo de la investigación en neurodegeneración.
1.1 La Doctrina de la Neurona: De una Red Enmarañada a un Huerto Elegante
El cambio de paradigma más monumental impulsado por Cajal fue el paso de la teoría reticular imperante, defendida por su rival Camillo Golgi, a su Doctrina de la Neurona. La teoría reticular postulaba que el sistema nervioso era una red continua y sincitial, una red ininterrumpida de fibras. Dentro de este modelo, el concepto de una enfermedad basada en la disfunción o muerte de células individuales era lógicamente insostenible; una patología tendría que afectar a toda la red simultáneamente, lo que no se corresponde con la naturaleza progresiva y regionalmente específica de la enfermedad de Alzheimer (EA).
Utilizando una versión modificada de la propia tinción de Golgi, Cajal demostró meticulosamente que el sistema nervioso estaba compuesto por células discretas e individuales: las neuronas. Este acto estableció a la neurona como la unidad fundamental anatómica, fisiológica, genética y, de manera crucial para este análisis, patológica del sistema nervioso. Esta doctrina es la “piedra angular” sobre la que se han construido todas las neurociencias, incluida la psiquiatría biológica y el estudio de la neurodegeneración. Sin ella, las patologías centrales del Alzheimer —la pérdida neuronal, la desconexión sináptica y la acumulación intraneuronal de ovillos— serían conceptualmente incoherentes. La propia idea de contar las neuronas perdidas o medir la densidad sináptica, prácticas estándar en la investigación de la EA, es una consecuencia directa de la teoría de Cajal. Su trabajo no solo aportó un descubrimiento científico, sino que supuso una revolución epistemológica que creó la propia posibilidad de estudiar enfermedades como el Alzheimer. Creó el lenguaje conceptual que permite formular la pregunta: “¿Qué causa la muerte de las neuronas en la enfermedad de Alzheimer?“.
1.2 Principios de Especificidad Conexional y Polarización Dinámica
Partiendo de la Doctrina de la Neurona, Cajal formuló principios posteriores que le dieron un significado funcional. La Ley de la Polarización Dinámica postulaba que los impulsos nerviosos fluyen en una dirección constante y predecible: desde las dendritas y el soma hacia el axón, y a través de un espacio especializado —la sinapsis— hasta la siguiente neurona.
Este concepto transformó el cerebro de una malla estática a un órgano dinámico de procesamiento de información compuesto por circuitos específicos. Proporciona el marco esencial para entender el Alzheimer no solo como una enfermedad de muerte celular, sino como un síndrome de desconexión progresiva. Las manifestaciones clínicas más tempranas, como la pérdida de memoria a corto plazo, se entienden ahora como el resultado del fallo de estas conexiones específicas (pérdida sináptica) en circuitos críticos como los del hipocampo, mucho antes de que se produzca una muerte neuronal generalizada. Los meticulosos dibujos de Cajal no eran meras ilustraciones, sino los primeros “diagramas de cableado” del cerebro. Este esfuerzo cartográfico proporcionó el mapa base de la normalidad contra el cual las alteraciones patológicas del Alzheimer pudieron ser cartografiadas posteriormente.
1.3 El Cerebro en Flujo: Conceptos Tempranos de Neuroplasticidad
Cajal albergaba ideas notablemente premonitorias sobre la capacidad del cerebro para cambiar, un concepto que denominó “gimnasia cerebral”. Propuso que el esfuerzo mental y el aprendizaje podían forjar conexiones más fuertes y numerosas entre las neuronas, superando la visión de un cerebro adulto fijo e inmutable.
Este concepto histórico se conecta directamente con la teoría moderna de la “reserva cognitiva”, que ayuda a explicar por qué los individuos con mayor nivel educativo u ocupaciones más complejas pueden tolerar una mayor carga de patología de Alzheimer antes de mostrar síntomas clínicos. La “gimnasia cerebral” de Cajal es el antecedente intelectual del principio de “úsalo o piérdelo” que sustenta muchos enfoques no farmacológicos para la prevención de la demencia. Su trabajo sentó las bases para todo el campo de la neuroplasticidad, un concepto ahora central para comprender tanto la vulnerabilidad del cerebro a la enfermedad como su potencial de resiliencia y reparación.
Sección 2: Degeneración y Regeneración: La Investigación Seminal de Cajal sobre la Patología Neuronal
Desde el estudio del cerebro sano, el análisis se desplaza ahora hacia las investigaciones igualmente profundas de Cajal sobre la patología. Su obra magna, Estudios sobre la degeneración y regeneración del sistema nervioso, es posiblemente el texto histórico más importante para comprender la dinámica celular de la enfermedad de Alzheimer. Proporciona un atlas detallado de cómo mueren las neuronas y, fundamentalmente, cómo intentan repararse a sí mismas.
2.1 Cartografiando la Decadencia Neuronal: Una Anatomía Sistemática de la Lesión
Cajal llevó a cabo estudios sistemáticos sobre las consecuencias de las lesiones mecánicas en todas las partes del sistema nervioso. Documentó meticulosamente la secuencia de eventos tras la sección de un axón, un proceso conocido como degeneración Walleriana. Sus descripciones de la fragmentación axonal, la formación de “mazas de crecimiento” terminales y los cambios reactivos en el soma neuronal proporcionan un paralelo morfológico directo con los procesos degenerativos observados en los cerebros con Alzheimer. Las neuritas distróficas, los esferoides axonales y las neuronas moribundas que se observan en la EA siguen las mismas reglas fundamentales de la patología que Cajal elucidó por primera vez a través de experimentos de trauma.
2.2 El Intento Abortivo: Brotación Regenerativa en el Sistema Nervioso Central
Este es el argumento central de la sección. El descubrimiento crucial y sombrío de Cajal fue que, mientras los nervios periféricos podían regenerarse, las neuronas del sistema nervioso central (SNC) adulto no podían hacerlo. Sin embargo, el genio de Cajal residió en observar que este no era un fracaso pasivo. Vio que las neuronas del SNC, cuando se lesionaban, producían nuevos brotes y conos de crecimiento, demostrando una capacidad intrínseca de regeneración. No obstante, estos intentos eran “efímeros, abortados y sin propósito”. Este fenómeno de “brotación abortiva” es una piedra angular de su obra.
Llegó a la conclusión de que el fracaso no se debía a una incapacidad inherente de la neurona para crecer, sino a un entorno inhóspito en el SNC que carecía de factores de apoyo y estaba lleno de obstáculos (la cicatriz glial). Esta distinción es profundamente importante y sigue siendo central en la neurociencia regenerativa moderna. Este trabajo revela una dualidad fundamental en la respuesta del cerebro al daño: un programa intrínseco de crecimiento que choca con un entorno extrínseco de inhibición. Esta concepción es directamente aplicable a la patología del Alzheimer, donde las neuritas distróficas que rodean las placas de amiloide no son solo signos pasivos de decadencia, sino la evidencia morfológica de la “brotación abortiva” de Cajal: neuronas que intentan activa pero inútilmente remodelarse y repararse en un entorno tóxico e inhibidor. Esto replantea la patología de una placa amiloide, pasando de ser una lápida estática a un campo de batalla dinámico.
2.3 La Hipótesis Neurotrópica: Una Llamada Química al Crecimiento y la Guía
Como corolario al problema de la regeneración fallida, Cajal propuso una solución: la hipótesis neurotrópica (inicialmente llamada “hipótesis quimiotáctica”). Postuló la existencia de sustancias químicas secretadas por las células diana (o, en la periferia, por las células de Schwann) que podían atraer y guiar a los axones en crecimiento. Este fue un constructo puramente teórico, nacido de la observación, que predijo la existencia de lo que ahora llamamos factores neurotróficos (por ejemplo, Factor de Crecimiento Nervioso (NGF), Factor Neurotrófico Derivado del Cerebro (BDNF)) y señales de guía (por ejemplo, Netrinas, Semaforinas).
Esta hipótesis proporcionó una explicación mecanicista tanto para el desarrollo exitoso como para la regeneración fallida. Razonó que el entorno del SNC carecía de estos cruciales “agentes catalíticos”, explicando así el fenómeno de la brotación abortiva.
Sección 3: Cajal se Enfrenta a la “Enfermedad Inusual”: Estudios Histopatológicos Directos
Esta sección presenta la evidencia concluyente de que Cajal no fue simplemente un precursor teórico, sino un investigador activo, aunque poco reconocido, de la enfermedad de Alzheimer. El descubrimiento de sus preparaciones histológicas lo reposiciona en la narrativa histórica.
3.1 Los Archivos del Museo Cajal: Redescubrimiento de una Investigación Olvidada
El notable descubrimiento de 37 preparaciones histológicas de pacientes con enfermedad de Alzheimer dentro de la colección personal de Cajal, ahora albergada en el Legado Cajal, es de una importancia capital. Este hallazgo demuestra que Cajal, un premio Nobel en la cima de su carrera, conocía el trabajo de Alzheimer y consideró la enfermedad lo suficientemente importante como para estudiarla personalmente, aplicando sus propias e inigualables técnicas de tinción y su ojo analítico al problema. Significativamente, esto ocurrió en el mismo año, 1906, en que Alzheimer presentó por primera vez sus hallazgos y Cajal recibió el premio Nobel, uniendo a los dos titanes en un momento histórico singular.
3.2 Una Lente Cajaliana sobre Placas y Ovillos
Mientras que Alzheimer describió las placas y los ovillos, el marco de Cajal permitió una interpretación mecanicista más profunda.
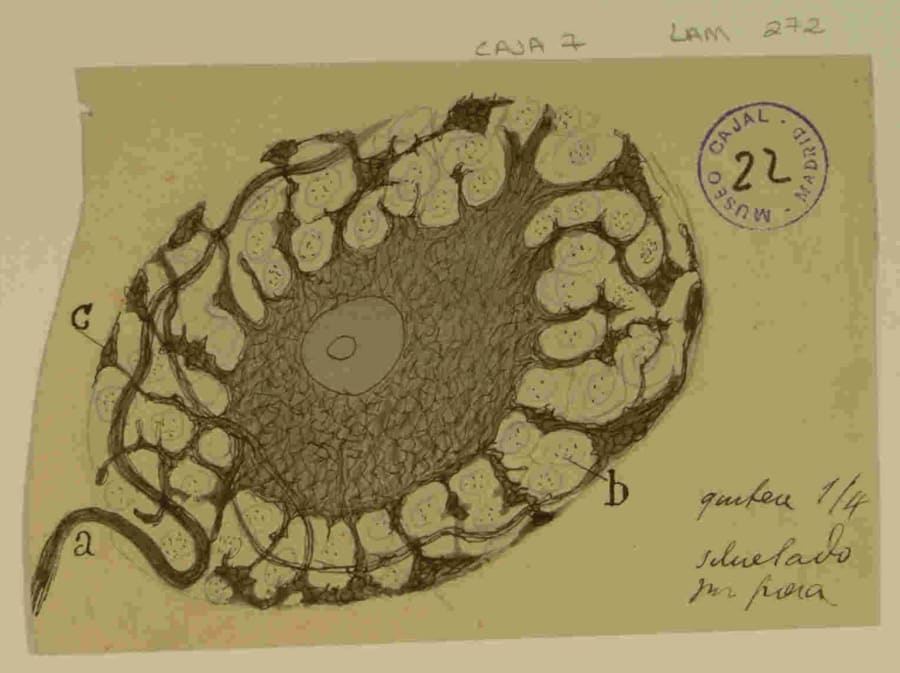
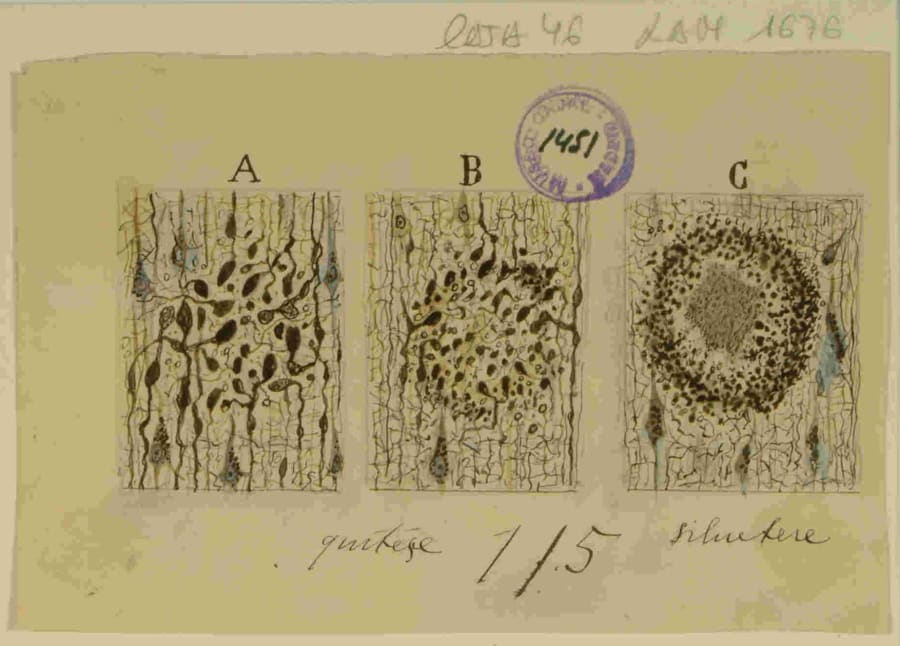
-
Ovillos Neurofibrilares: En la época, estas estructuras eran conocidas como “lesiones de Alzheimer”. Cajal las habría visto como una profunda alteración de la estructura neurofibrilar que había pasado décadas estudiando. Representarían un colapso del citoesqueleto interno, esencial para mantener la forma y la función neuronal, lo que inevitablemente conduciría a la muerte de la neurona.
-
Placas Seniles: Aquí reside la clave de la aportación de Cajal. Mientras que otros veían la placa como la lesión primaria, el enfoque de Cajal se habría centrado en los procesos neuronales alrededor de la placa. Las neuritas hinchadas, distorsionadas y en brotación (neuritas distróficas) que rodean el núcleo de amiloide habrían sido, para él, una confirmación perfecta in vivo de su teoría de la “brotación abortiva”. No las habría visto como víctimas pasivas de la placa, sino como conos de crecimiento y axones activos y luchadores que intentaban navegar por un terreno tóxico e intransitable, para finalmente fracasar y degenerar. Además, Cajal ya había observado la presencia de placas amiloides en los cerebros de algunas personas mayores sanas, lo que sugería una relación más compleja que una simple causalidad.
Las neuritas distróficas que rodean las placas seniles son la manifestación física donde convergen las dos grandes teorías de Cajal: la Doctrina de la Neurona y la Regeneración Abortiva. Representan a la neurona individual (Doctrina) intentando y fracasando en su intento de repararse a sí misma (Regeneración Abortiva). Para Cajal, la placa senil no era solo un marcador de enfermedad, sino un teatro microscópico que exhibía la tragedia central de la patología del SNC que él ya había definido: la lucha heroica pero condenada de la neurona por sobrevivir.

3.3 Historia de Dos Titanes: Comparando los Enfoques de Cajal y Alzheimer
Es fundamental realizar una comparación matizada para clarificar sus roles distintos pero complementarios. Alois Alzheimer fue un brillante clínico y neuropatólogo. Su genio residió en vincular un síndrome clínico específico (demencia progresiva) con un conjunto específico de hallazgos microscópicos (placas y ovillos), definiendo así una nueva entidad nosológica. Su enfoque fue fundamentalmente descriptivo y correlacional.
Cajal, en cambio, fue un biólogo fundamental. Su contribución no fue definir la enfermedad, sino proporcionar el marco mecanicista para entenderla. Proporcionó las leyes biológicas —la Doctrina de la Neurona, los principios de la degeneración, el fracaso de la regeneración— que explicaban por qué la presencia de placas y ovillos conduciría inevitablemente a la pérdida catastrófica de la memoria y la cognición. Su enfoque fue mecanicista y explicativo.
CaracterísticaAlois AlzheimerSantiago Ramón y Cajal****Enfoque PrincipalCorrelación Clínico-PatológicaMecanismos Biológicos FundamentalesDescubrimiento ClaveDescripción de una nueva entidad nosológica que vincula la demencia con placas y ovillosElucidación de la neurona como unidad básica y las leyes de su función, degeneración y regeneración fallidaMarco TeóricoDescriptivo: “¿Qué es esta enfermedad?”Mecanicista: “¿Cómo funciona y se daña el sistema nervioso?”Interpretación de Placas/OvillosSellos patológicos que definen la enfermedad Focos de citopatología neuronal; evidencia de colapso citoesquelético (ovillos) y brotación regenerativa abortiva (neuritas distróficas alrededor de las placas)Legado DuraderoEpónimo de la enfermedad; pionero de la neuropatología clínicaPadre de la neurociencia; proveedor del conjunto de herramientas conceptuales para entender los mecanismos de la enfermedad
3.4 La Escuela de Cajal y el Puente de Achúcarro
El legado de Cajal no se limita a su propia obra, sino que se extiende a través de la influyente “Escuela de Cajal”, una generación de discípulos que aplicaron y expandieron sus teorías. Entre ellos, Nicolás Achúcarro (1880-1918) emerge como una figura crucial, actuando como un puente intelectual entre el laboratorio de Cajal y el de Alois Alzheimer. Achúcarro no solo fue un discípulo aventajado de Cajal, sino que también trabajó directamente con Alzheimer en Múnich, ganándose su profundo respeto hasta el punto de que Alzheimer lo recomendó para dirigir un importante laboratorio en Washington D.C..

Mientras Cajal se centraba en la neurona, Achúcarro dirigió su atención a la neuroglía, las células no neuronales que Cajal había agrupado bajo el término “tercer elemento”. Fue un pionero en el estudio de estas células, desarrollando, a veces con la ayuda del propio Cajal, nuevas técnicas de tinción para visualizarlas específicamente. Su trabajo fue fundamental para identificar la microglía como células con capacidad fagocítica, es decir, capaces de “limpiar” los desechos celulares. Esta observación es de una importancia capital para la enfermedad de Alzheimer, donde hoy se sabe que la microglía se agrupa de forma reactiva alrededor de las placas seniles.
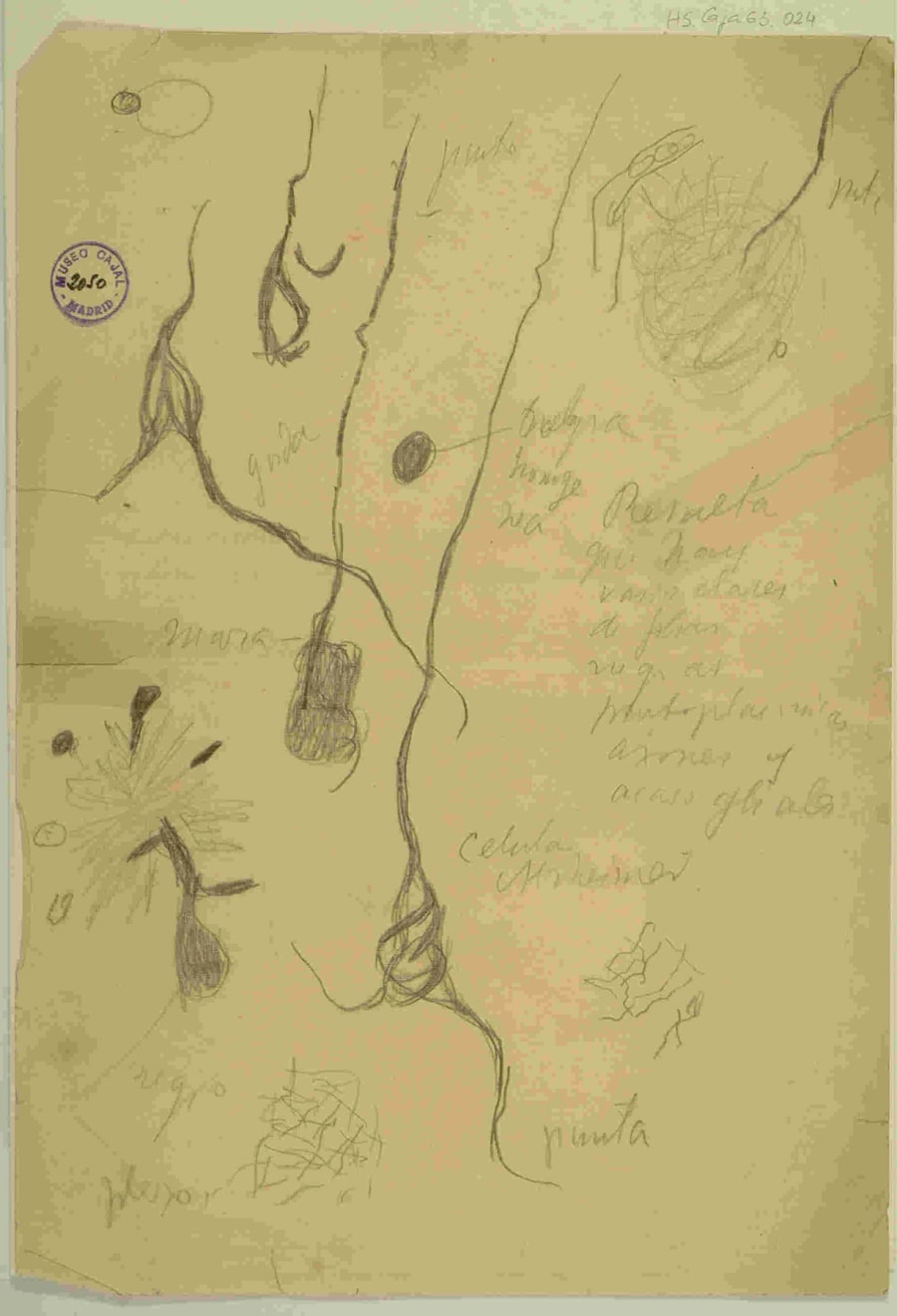
Las contribuciones de Achúcarro a la demencia fueron directas y significativas. Publicó sobre la anatomía patológica de la demencia senil y, de forma notable, describió un caso de demencia que presentaba ovillos neurofibrilares pero carecía de placas. En este contexto, fue el primero en describir inclusiones fibrilares gliales, a las que llamó “anillos” y “cestas”, demostrando una comprensión de la patología que iba más allá de la neurona e implicaba a las células gliales en el proceso degenerativo. Considerado por muchos como el sucesor natural de Cajal, la prematura muerte de Achúcarro a los 37 años truncó una carrera brillante que ya había conectado de forma indeleble los principios fundamentales de la neurobiología de Cajal con la neuropatología clínica de Alzheimer.
Sección 4: El Legado Perdurale: La Influencia de Cajal en la Investigación del Alzheimer del Siglo XXI
El trabajo de Cajal no es una mera curiosidad histórica, sino una influencia viva en la investigación contemporánea del Alzheimer. Es posible trazar líneas directas y explícitas desde sus conceptos de finales del siglo XIX y principios del XX hasta las estrategias terapéuticas del siglo XXI.
4.1 De la Brotación Abortiva a los Esferoides Axonales: Visiones Modernas de la Distrofia Asociada a la Placa
Los dibujos de Cajal de las “mazas de crecimiento” y las neuritas distróficas se conectan directamente con la investigación moderna sobre los “esferoides axonales”. Estos esferoides, que ahora se entienden como sitios de transporte axonal deficiente y acumulación de orgánulos alrededor de las placas, son la visión moderna y de alta resolución de las mismas estructuras patológicas que Cajal identificó por primera vez hace más de un siglo. La investigación actual que se dirige a estos esferoides como una estrategia terapéutica, independientemente de la eliminación del amiloide, puede verse como un intento directo de resolver el problema de la brotación abortiva que Cajal observó. Esto demuestra que su enfoque en la reacción neuronal a la placa, en lugar de la placa en sí, fue notablemente premonitorio.
4.2 Aprovechando el Neurotropismo: La Búsqueda Continua de Terapias Regenerativas
Existe un linaje directo desde la hipótesis neurotrópica de Cajal hasta el campo moderno de la medicina regenerativa para las enfermedades neurodegenerativas. La búsqueda de terapias que utilizan factores neurotróficos (NGF, BDNF), células madre que secretan estos factores o terapias génicas para aumentar su producción es el cumplimiento directo del llamado de Cajal a suministrar al SNC los “agentes catalíticos” de los que carece. La investigación actual se basa explícita o implícitamente en este principio cajaliano: que apoyar la salud neuronal y promover un entorno permisivo para el crecimiento es una vía terapéutica clave.
El marco de Cajal de hace un siglo, que contrapone un “entorno inhibidor” a un “potencial regenerativo intrínseco”, sigue siendo una heurística poderosa y precisa para clasificar y comprender todo el panorama de la investigación terapéutica moderna sobre el Alzheimer. Las estrategias actuales pueden dividirse en dos grandes categorías que intentan resolver los dos problemas fundamentales identificados por Cajal: (A) eliminar la inhibición ambiental (por ejemplo, terapias anti-amiloide o anti-tau) o (B) reforzar la capacidad regenerativa intrínseca de la neurona (por ejemplo, terapias con factores neurotróficos). Su trabajo proporciona la dicotomía intelectual fundamental que todavía define el campo.
4.3 La Doctrina de la Neurona Revisitada: El Alzheimer como una Enfermedad de Fallo Sináptico y Colapso de Redes
La concepción moderna más avanzada del Alzheimer —como una “sinaptopatía” donde la disfunción y la pérdida sináptica preceden a la muerte celular en años o incluso décadas— es la reivindicación última de los principios fundacionales de Cajal. Si la neurona es la unidad individual y la sinapsis es el punto de contacto, entonces el punto de fallo más temprano en un circuito complejo será la sinapsis. La pérdida de memoria y función cognitiva en la EA es el resultado directo de este colapso sináptico, una manifestación funcional de la ruptura de los principios de Cajal sobre la polarización dinámica y la conectividad específica. Esta visión moderna valida el enfoque de Cajal en la neurona y sus conexiones como el locus primario de la función y, por extensión, de la disfunción del sistema nervioso.
Sección 5: Fronteras Actuales en la Investigación y Tratamiento del Alzheimer
Sobre los cimientos establecidos por pioneros como Cajal y Alzheimer, la ciencia del siglo XXI ha logrado avances significativos en la comprensión de la enfermedad de Alzheimer, abriendo nuevas vías para el diagnóstico y el tratamiento.
5.1 Comprensión Actual de los Mecanismos de la Enfermedad
La visión moderna de la EA es la de una enfermedad multifactorial compleja. Si bien las placas de beta-amiloide y los ovillos de la proteína tau siguen siendo las características patológicas centrales, ahora se entiende que son parte de una cascada más amplia de eventos.
-
Patología Amiloide y Tau: La hipótesis amiloide postula que la acumulación de péptidos beta-amiloide fuera de las neuronas es un evento iniciador clave. Estos agregados interfieren con la comunicación sináptica y desencadenan procesos inflamatorios. Dentro de la neurona, la proteína tau, que normalmente estabiliza los microtúbulos, se hiperfosforila y forma ovillos neurofibrilares. Esto desintegra el sistema de transporte de la neurona, lo que lleva a la disfunción y, finalmente, a la muerte celular.
-
Disfunción Sináptica: De acuerdo con los principios de Cajal, la investigación actual enfatiza que la pérdida de sinapsis es una de las características más tempranas y el mejor correlato del deterioro cognitivo, ocurriendo mucho antes de la muerte neuronal generalizada.
-
Neuroinflamación: Las células inmunitarias del cerebro, como la microglía, se activan en respuesta a las placas amiloides. Si bien esta respuesta puede ser inicialmente protectora, la activación crónica libera mediadores proinflamatorios que contribuyen al daño neuronal.
-
Factores Genéticos y de Estilo de Vida: Se han identificado múltiples factores de riesgo. Las mutaciones en genes como APP, PSEN1 y PSEN2 causan formas raras de inicio temprano, mientras que la variante APOE-e4 es el principal factor de riesgo genético para la forma tardía más común. Además, factores como la diabetes, la obesidad, la inactividad física y el aislamiento social se asocian con un mayor riesgo.
5.2 Avances en el Diagnóstico Precoz
El diagnóstico de la EA ha evolucionado desde una evaluación puramente clínica de los síntomas a un enfoque basado en biomarcadores que pueden detectar la enfermedad en sus etapas más tempranas, incluso antes de que aparezcan los síntomas.
-
Neuroimagen: Las técnicas de imagen cerebral son fundamentales. La resonancia magnética (RM) y la tomografía computarizada (TC) pueden mostrar la atrofia cerebral, especialmente en regiones como el hipocampo. Las tomografías por emisión de positrones (TEP) permiten visualizar directamente las placas de amiloide y los ovillos de tau en el cerebro de personas vivas, confirmando la patología subyacente.
-
Biomarcadores en Fluidos: El análisis del líquido cefalorraquídeo (LCR) puede medir los niveles de beta-amiloide y proteína tau, reflejando los cambios que ocurren en el cerebro. Más recientemente, el desarrollo de análisis de sangre de alta sensibilidad para detectar estas mismas proteínas y otros marcadores representa un avance revolucionario, ofreciendo una herramienta menos invasiva y más accesible para el diagnóstico temprano y el seguimiento de la enfermedad.
5.3 Nuevos Horizontes Terapéuticos
Aunque todavía no existe una cura, el panorama terapéutico está cambiando rápidamente, pasando de medicamentos que solo tratan los síntomas a terapias que modifican la enfermedad.
-
Terapias Anti-Amiloide: La investigación ha llevado al desarrollo de anticuerpos monoclonales diseñados para eliminar las placas de beta-amiloide del cerebro. Varios de estos fármacos han sido aprobados y han demostrado la capacidad de ralentizar la progresión del deterioro cognitivo en las primeras etapas de la enfermedad.
-
Terapias dirigidas a Tau y la Inflamación: Se están investigando activamente otras dianas terapéuticas. Esto incluye medicamentos que buscan prevenir la agregación de la proteína tau o eliminar los ovillos ya formados, así como fármacos que modulan la respuesta neuroinflamatoria para reducir su impacto dañino.
-
Medicina Regenerativa y Neuroprotección: En línea con las ideas de Cajal sobre la regeneración, las estrategias futuras exploran el uso de factores neurotróficos para apoyar la supervivencia de las neuronas y el uso de células madre para reemplazar las células perdidas o crear un entorno más propicio para la reparación.
-
Prevención y Estilo de Vida: Existe un creciente reconocimiento de que la modificación de los factores de riesgo del estilo de vida, como la dieta, el ejercicio y la actividad cognitiva, puede desempeñar un papel importante en la reducción del riesgo de desarrollar demencia.
Sección 6: Propósito de Vida y Resiliencia Cerebral: Una Nueva Frontera en la Prevención del Alzhéimer
6.1 Deconstruyendo el Enigma de la Enfermedad de Alzhéimer
Para dimensionar el poder de la prevención, es imperativo comprender la naturaleza de la amenaza. La enfermedad de Alzheimer no es una consecuencia ineludible del envejecimiento, sino un trastorno neurodegenerativo específico, con una biología, una epidemiología y un conjunto de factores de riesgo bien definidos.
6.1.1 El Cerebro Bajo Asedio: La Neuropatología de la Enfermedad de Alzhéimer
La enfermedad de Alzheimer es un trastorno cerebral progresivo que destruye de forma inexorable la memoria y las capacidades cognitivas, constituyendo la causa más común de demencia. Representa entre el 50% y el 75% de todos los casos de demencia, una patología que se distingue cualitativamente de los olvidos ocasionales asociados al envejecimiento fisiológico.
A nivel microscópico, el cerebro afectado por el alzhéimer se caracteriza por dos sellos patológicos distintivos. El primero son las placas de beta-amiloide, depósitos extracelulares de fragmentos proteicos que se agregan en los espacios sinápticos, interfiriendo con la comunicación neuronal. El segundo son los ovillos neurofibrilares, formados por una versión hiperfosforilada de la proteína tau que se acumula en el interior de las neuronas, desestabilizando su citoesqueleto. Si las neuronas fueran fábricas, las placas amiloides actuarían como residuos que bloquean las vías de suministro externas, mientras que los ovillos de tau serían como maquinaria interna que se deforma y colapsa, saboteando la producción. Este doble asalto patológico interrumpe la neurotransmisión, desencadena una respuesta neuroinflamatoria crónica y, en última instancia, conduce a una muerte celular programada (apoptosis) a gran escala, resultando en una atrofia macroscópica del tejido cerebral.
Clínicamente, este proceso biológico se manifiesta en una progresión devastadora. Se inicia con síntomas sutiles, como la dificultad para recordar eventos recientes, que a menudo se confunden con el envejecimiento normal. Conforme la enfermedad avanza, el daño se extiende a áreas cerebrales que controlan el lenguaje, el razonamiento y el procesamiento sensorial. Los pacientes pueden experimentar desorientación en entornos familiares, agnosia (dificultad para reconocer a seres queridos) y alteraciones conductuales y de la personalidad, como ansiedad o agresividad. En sus fases terminales, la enfermedad culmina en una dependencia total, borrando la capacidad de realizar las funciones más básicas de autocuidado.
6.1.2 La Progresión Clínica: Las Siete Fases del Alzheimer
Para contextualizar la devastadora progresión clínica de la enfermedad, es útil recurrir a la Escala Global del Deterioro (GDS), un estándar utilizado mundialmente para clasificar su evolución en siete fases.
-
Fase 1: Sin deterioro cognitivo aparente. La persona no experimenta problemas de memoria y se encuentra mentalmente sana.
-
Fase 2: Deterioro cognitivo muy leve. Se manifiestan los primeros olvidos, a menudo atribuidos al envejecimiento normal (p. ej., olvidar nombres o dónde se dejan las llaves). La función cognitiva general no se ve afectada.
-
Fase 3: Deterioro cognitivo leve (DCL). Los déficits se vuelven más evidentes para familiares y amigos. La persona puede tener dificultades para encontrar la palabra correcta, recordar nombres de personas que acaba de conocer, planificar u organizar, y pierde o extravía objetos con frecuencia. La ansiedad ante estos síntomas es común.
-
Fase 4: Deterioro cognitivo moderado (Demencia leve). En esta etapa, el diagnóstico de alzhéimer puede realizarse con precisión. Los problemas de memoria a corto plazo son evidentes, y la persona puede tener dificultades con tareas complejas como gestionar sus finanzas, preparar una comida o recordar su historia personal. A menudo, la persona se retrae socialmente y puede mostrar un estado de ánimo apático.
-
Fase 5: Deterioro cognitivo moderadamente grave (Demencia moderada). La persona ya no puede vivir de forma independiente y necesita ayuda con actividades cotidianas. Las lagunas de memoria son significativas; puede no recordar su dirección o número de teléfono y confundirse sobre la fecha o el lugar en el que se encuentra. Sin embargo, generalmente aún reconoce a sus familiares cercanos y recuerda detalles de su pasado.
-
Fase 6: Deterioro cognitivo grave (Demencia moderadamente grave). La memoria empeora drásticamente y pueden surgir cambios significativos en la personalidad. La persona necesita ayuda extensa con las actividades básicas de la vida diaria, como vestirse, ir al baño y comer. Puede deambular, volverse incontinente y experimentar ansiedad, agitación o delirios. El reconocimiento de los seres queridos se vuelve cada vez más difícil.
-
Fase 7: Deterioro cognitivo muy grave (Demencia grave). En la fase final de la enfermedad, la persona pierde la capacidad de responder a su entorno, de hablar y, finalmente, de controlar el movimiento. Necesita asistencia continua para todas las actividades básicas. La rigidez muscular es común y la capacidad de tragar se ve comprometida, lo que a menudo conduce a complicaciones como la neumonía por aspiración.
6.1.3 Una Crisis Anunciada: El Imperativo Epidemiológico en España y el Mundo
Las proyecciones demográficas dibujan un panorama alarmante. En España, la Fundación de Ciencias de la Salud advierte que, en ausencia de medidas preventivas eficaces, el número de personas con algún tipo de demencia podría alcanzar los dos millones para el año 2050. Otras estimaciones son aún más graves, proyectando que solo los casos de alzhéimer podrían superar los 3.6 millones en España para esa fecha, triplicando las cifras actuales. Esta enfermedad ya se sitúa entre las principales causas de muerte y es la principal causa de dependencia en la población anciana, con un coste por paciente que puede oscilar entre 27,000 y 37,000 euros anuales, una carga económica asumida en un 87% por las familias.
Este desafío trasciende las fronteras nacionales. A nivel mundial, se prevé que el número de personas con demencia se triplique para 2050, pasando de los 55.2 millones estimados en 2019 a 139 millones. Esta escalada representa una crisis sanitaria, social y económica de proporciones globales, subrayando la urgencia universal de identificar y promover estrategias de prevención efectivas.
6.1.4 El Paisaje del Riesgo: Diferenciando el Determinismo Genético de los Factores Modificables
Durante décadas, la narrativa en torno al alzhéimer estuvo dominada por un cierto fatalismo, una percepción de la enfermedad como una sentencia dictada por la edad y la herencia genética. Si bien estos factores son innegablemente relevantes, la ciencia moderna ha revelado una imagen mucho más matizada y esperanzadora.
Los principales factores de riesgo no modificables son la edad, que sigue siendo el más significativo, y la genética. El factor genético más influyente para el alzhéimer de inicio tardío es el gen de la Apolipoproteína E (APOE). Este gen presenta tres variantes comunes: APOE-e2, que parece conferir cierta protección; APOE-e3, la variante más común y de efecto neutro; y APOE-e4, que incrementa significativamente el riesgo de desarrollar la enfermedad. Es crucial entender que APOE-e4 es un gen de susceptibilidad, no un gen determinista. Portar una o incluso dos copias de este alelo aumenta la probabilidad, pero no garantiza el desarrollo de la enfermedad; de hecho, entre el 40% y el 65% de las personas diagnosticadas con alzhéimer portan al menos una copia del alelo APOE-e4. Los genes deterministas (como APP, PSEN1 y PSEN2), que sí causan la enfermedad de forma casi inevitable, son extremadamente raros y responsables de formas de alzhéimer familiar de inicio temprano, representando menos del 1% de todos los casos.
El avance más significativo en la comprensión del riesgo ha sido el reconocimiento del enorme peso de los factores modificables. Informes de referencia, como el de la Comisión Lancet de 2024, estiman que hasta un 40-45% de los casos de demencia podrían prevenirse o retrasarse mediante la intervención sobre un conjunto de factores de riesgo a lo largo de la vida. Estos incluyen un bajo nivel educativo, hipertensión, pérdida auditiva, tabaquismo, obesidad, depresión, inactividad física, diabetes, aislamiento social, consumo excesivo de alcohol y exposición a la contaminación del aire.
Esta revelación marca un cambio de paradigma fundamental. El alzhéimer ya no se percibe como un destino genético ineludible, sino como una condición contra la cual se puede luchar activamente. El miedo que ha paralizado a generaciones está empezando a disiparse, no por la existencia de una cura milagrosa, sino porque el locus de control se está desplazando. La ciencia ha devuelto la agencia a los individuos y a los sistemas de salud pública, transformando la conversación de una de gestión pasiva a una de prevención proactiva y empoderamiento. Es en este nuevo y esperanzador contexto donde la investigación sobre el propósito vital adquiere una relevancia extraordinaria.
6.1.5 El Legado de Cajal y la Escuela Española de Neurología: Los Cimientos de la Investigación en Demencia
Mucho antes de que la enfermedad de Alzheimer se convirtiera en una crisis de salud pública global, Santiago Ramón y Cajal y sus discípulos sentaron las bases para su comprensión. Aunque el término “enfermedad de Alzheimer” fue acuñado por sus contemporáneos alemanes, la labor de la Escuela Española de Neurología fue fundamental para describir las alteraciones celulares que definen esta y otras demencias.
El propio Cajal, con su característica agudeza, reflexionó sobre el declive cognitivo en la vejez, lo que él denominaba “memoria senil”. En sus escritos, lamentaba:
“por desdicha nuestra, tan preciosa propiedad del cerebro (la memoria) flaquea lamentablemente en la senectud”.
Su trabajo más importante, la “doctrina de la neurona”, que postulaba que el sistema nervioso estaba compuesto por células individuales y no por una red continua, fue el pilar conceptual que permitió entender la neurodegeneración como un proceso de muerte celular. De hecho, entre su vasto legado de preparaciones histológicas y dibujos magistrales, se encuentran observaciones directas de la “degeneración en demencia precoz”.
Tras la concesión del Premio Nobel en 1906, el prestigio de Cajal atrajo a una pléyade de jóvenes médicos, dando lugar a la “Escuela Neurohistológica de Cajal”. Este grupo, del que formaban parte numerosos psiquiatras y neurólogos, estaba imbuido de la convicción de que la base de las enfermedades mentales residía en alteraciones morfológicas del cerebro, un principio que guio sus investigaciones. Entre sus discípulos más destacados en este campo se encuentran:
-
Nicolás Achúcarro (1880-1918): Considerado uno de los discípulos más brillantes, Achúcarro se formó directamente con Alois Alzheimer en Múnich. Fue pionero en el estudio de la neuroglía, las células de soporte del sistema nervioso, y describió su implicación en la formación de las placas seniles. Junto a Lafora, fue uno de los primeros en describir casos de la enfermedad de Alzheimer en Norteamérica.
-
Pío del Río-Hortega (1882-1945): Su contribución fue monumental. A partir del “tercer elemento” celular que Cajal no había logrado definir completamente, Río-Hortega identificó y caracterizó dos tipos celulares cruciales: la oligodendroglía y, fundamentalmente, la microglía. Describió la microglía como las células inmunitarias residentes del cerebro, con capacidad fagocítica para eliminar desechos. Este descubrimiento fue profético; hoy sabemos que la disfunción de la microglía y la neuroinflamación son procesos centrales en la patogénesis de la enfermedad de Alzheimer.
-
Gonzalo Rodríguez Lafora (1886-1971): También formado con Alzheimer, Lafora realizó aportaciones cruciales. Describió dos de los primeros casos de la enfermedad en Estados Unidos, estudiando apasionadamente la histopatología de las “psicosis seniles y preseniles”. Sus observaciones fueron de una precisión asombrosa: describió las fases sucesivas de la formación de las placas, la mayor abundancia de degeneración neurofibrilar en el córtex occipital y la existencia de la degeneración granulovacuolar de las neuronas. Además, en 1911, identificó la enfermedad que lleva su nombre, una forma de epilepsia mioclónica progresiva que cursa con una demencia devastadora, caracterizada por la presencia de los “cuerpos de Lafora”.
En conjunto, el trabajo de Cajal y su escuela no solo estableció la neurona como la unidad funcional del sistema nervioso, sino que también inició el estudio sistemático de las alteraciones celulares —neuronales y gliales— que subyacen a la demencia. Su legado demuestra que, desde sus inicios, la ciencia española ha estado en la vanguardia de la lucha por descifrar los misterios del cerebro envejecido.
6.2 El Poder del Propósito: De la Hipótesis a la Evidencia Científica
La idea de que una vida con sentido puede proteger el cerebro, inspirada por comunidades como las de las Zonas Azules, ha pasado del ámbito de la observación anecdótica al de la investigación científica rigurosa. Un estudio reciente ha cuantificado este efecto, mientras que otras investigaciones empiezan a desvelar los mecanismos neurobiológicos subyacentes.
6.2.1 Un Estudio de Referencia: Cuantificando el Efecto Protector del Significado
Un estudio fundamental publicado en la edición de octubre de 2025 de The American Journal of Geriatric Psychiatry por Nicholas C. Howard, Aliza P. Wingo y colaboradores, proporciona la evidencia más sólida hasta la fecha sobre la conexión entre el propósito vital y la salud cognitiva.
La robustez del estudio se basa en su rigurosa metodología. Los investigadores utilizaron datos del Health and Retirement Study, una cohorte estadounidense grande y representativa a nivel nacional, siguiendo a 13,765 adultos mayores de 45 años durante un período de hasta 15 años (con una mediana de 8 años). El “Propósito en la Vida” (PiL, por sus siglas en inglés) no se midió de forma vaga, sino a través de un cuestionario validado de siete ítems de las Medidas de Bienestar Psicológico de Ryff, que evalúa afirmaciones como “Tengo un sentido de dirección y propósito en mi vida”, generando una puntuación cuantitativa. La salud cognitiva se evaluó objetivamente cada dos años mediante una prueba telefónica estandarizada, el modified Telephone Interview for Cognitive Status (mTICS).
Los resultados fueron contundentes. Las personas con una puntuación más alta en propósito vital tenían un riesgo aproximadamente un 28% menor de desarrollar deterioro cognitivo (ya fuera deterioro cognitivo leve o demencia) en comparación con aquellas con un propósito vital más bajo (Hazard Ratio = 0.72). De manera crucial, este efecto protector se mantuvo incluso después de ajustar estadísticamente por factores de riesgo conocidos como el nivel educativo, los síntomas depresivos y, notablemente, la presencia del factor de riesgo genético APOE-e4.
Además, el estudio reveló que un mayor propósito vital se asociaba con una aparición más tardía del deterioro cognitivo. Aunque el retraso promedio fue de 1.4 meses durante el período de seguimiento, una cifra que a primera vista puede parecer modesta, su verdadera importancia se revela al compararla con las alternativas farmacéuticas actuales. Fármacos anti-amiloides, que también ofrecen un retraso modesto en la progresión de los síntomas, conllevan costes económicos elevados y riesgos significativos de efectos secundarios graves, como edema y hemorragias cerebrales. En contraste, como señalan los propios investigadores, cultivar un propósito en la vida es una intervención “gratuita, segura y accesible para todos”. El valor de este hallazgo no reside en la magnitud absoluta del retraso, sino en su incomparable perfil de riesgo-beneficio y su aplicabilidad universal, lo que lo convierte en un descubrimiento de primer orden para la salud pública.
Métrica****Hallazgo ClavePoblación de Estudio>13,000 adultos (edad ≥ 45 años) del U.S. Health and Retirement Study.Duración del SeguimientoHasta 15 años.Resultado PrincipalUn mayor Propósito en la Vida (PiL) se asoció con un riesgo ~28% menor de desarrollar deterioro cognitivo.Interacción GenéticaEl efecto protector del PiL persiste incluso en individuos con el factor de riesgo genético APOE-e4.Retraso en la ApariciónUn mayor PiL se asoció con un retraso promedio de 1.4 meses en la aparición del deterioro cognitivo.Limitación ClaveEl estudio demuestra una fuerte asociación, pero no prueba una relación de causalidad.
6.2.2 La Neurobiología de una Vida con Propósito: Construyendo un Cerebro Resiliente
La pregunta que surge de estos hallazgos es: ¿cómo puede un estado psicológico influir en la biología del cerebro? La respuesta parece residir en los conceptos de reserva cognitiva y resiliencia cerebral. La reserva cognitiva es la capacidad del cerebro para tolerar un mayor grado de patología (como placas amiloides) sin que se manifiesten síntomas clínicos. Tradicionalmente, se ha considerado que esta reserva se construye a través de la educación y la estimulación cognitiva a lo largo de la vida.
La evidencia emergente sugiere que el propósito vital es un potente constructor de esta reserva. Una vida con propósito no es pasiva; implica inherentemente establecer metas, planificar, resolver problemas y participar en actividades complejas, todas ellas tareas que fortalecen las redes neuronales. Más allá de ser un simple motivador de conductas saludables, el propósito podría ser un agente neurobiológico directo del cambio.
Investigaciones de la Barcelona Brain Health Initiative (BBHI) proporcionan un posible mecanismo. Un estudio de este grupo encontró que, en adultos de mediana edad, un mayor propósito en la vida (denominado “plan vital”) promovía la resiliencia contra el impacto negativo de las lesiones de la sustancia blanca en las funciones ejecutivas. El hallazgo más revelador fue que las personas con un propósito más alto mostraban una mayor integración funcional de la red neuronal por defecto (DMN, por sus siglas en inglés), un circuito cerebral clave. Esto sugiere que el estado psicológico de tener un propósito puede influir directamente en la plasticidad cerebral, esculpiendo una arquitectura de red más eficiente y robusta. Este “cerebro mejor cableado” puede compensar mejor el daño patológico, retrasando la aparición de los síntomas. Por lo tanto, el propósito no es solo un catalizador de hábitos saludables; es un “entrenamiento” para circuitos cerebrales específicos, construyendo activamente la resiliencia a nivel biológico.
Adicionalmente, un propósito vital actúa como un amortiguador psicológico contra el estrés crónico, el cual está asociado con niveles elevados de cortisol y neuroinflamación, ambos perjudiciales para la salud cerebral. La espiritualidad y la fe, fuentes comunes de propósito, se han relacionado específicamente con niveles más bajos de proteínas asociadas al estrés, lo que podría tener efectos neuroprotectores directos.
6.2.3 Ikigai: Un Modelo Cultural para el Propósito
El concepto japonés de “ikigai” (生き甲斐) ofrece un marco cultural que encapsula perfectamente la esencia de una vida con propósito. Traducido como “la razón de ser” o “el motivo por el que te levantas por la mañana”, el ikigai es un principio central en la longevidad de la Zona Azul de Okinawa.
El ikigai se conceptualiza a menudo como la intersección de cuatro elementos fundamentales:
-
Lo que amas (tu pasión).
-
En lo que eres bueno (tu vocación).
-
Lo que el mundo necesita (tu misión).
-
Por lo que te pueden pagar (tu profesión).
Encontrar el punto donde estos cuatro círculos se superponen es encontrar el ikigai. Este modelo no solo proporciona una hoja de ruta para identificar un propósito, sino que también valida culturalmente los hallazgos científicos, demostrando que la búsqueda de un significado ha sido, durante mucho tiempo, un pilar de las comunidades más longevas y saludables del mundo.
6.3 Los Pilares de la Longevidad Cognitiva: Un Marco Basado en la Evidencia
Si un propósito vital es el motor de la resiliencia cerebral, ¿cuáles son las conductas y hábitos que lo manifiestan en el día a día? La investigación ha identificado cinco pilares interconectados que, en conjunto, forman un ecosistema de salud cerebral. Estos pilares no son simplemente una lista de tareas; son la expresión tangible de una vida con significado y dirección.
6.3.1 Pilar 1: La Sinapsis Social—Cultivando Conexiones Profundas
El aislamiento social es un factor de riesgo bien establecido para el deterioro cognitivo. Múltiples revisiones sistemáticas y metaanálisis confirman que las relaciones sociales deficientes, tanto en cantidad (tamaño de la red) como en calidad (apoyo percibido), se asocian con un mayor riesgo de declive cognitivo. Por el contrario, una alta participación en actividades sociales se correlaciona con mejores resultados cognitivos.
El mecanismo protector es doble. Por un lado, la interacción social es una de las actividades cognitivamente más exigentes que realizamos, requiriendo atención, memoria, función ejecutiva y procesamiento del lenguaje en tiempo real. Esto fortalece los circuitos neuronales bajo el principio de “úsalo o piérdelo”. Por otro lado, las redes sociales sólidas proporcionan un apoyo emocional crucial que actúa como amortiguador contra el estrés, un conocido neurotóxico. El propósito vital a menudo se encuentra y se expresa a través de estas conexiones, como cuidar de la familia o pasar tiempo con los nietos, actividades que el estudio de Howard et al. identificó como fuentes de significado.
6.3.2 Pilar 2: La Mente Activa—Construyendo Reserva a Través del Compromiso Vitalicio
El cerebro, como un músculo, se beneficia del ejercicio constante. La evidencia es clara: el aprendizaje continuo a lo largo de la vida está asociado con una mejor función cognitiva, independientemente del nivel educativo alcanzado en la juventud. Un estudio de la Universidad de Duke encontró que la función cognitiva de una persona de 71 años que participa en actividades de aprendizaje es comparable a la de una persona promedio de 65 años.
La clave es la estimulación a través de la novedad y el desafío. Participar en actividades mentalmente estimulantes, como leer, aprender un nuevo idioma, desarrollar un hobby o participar en talleres, se asocia con una reducción significativa del riesgo de demencia. Incluso la complejidad cognitiva del trabajo de una persona puede tener un efecto protector a largo plazo.
El acto de establecer y perseguir metas personales es una forma particularmente poderosa de estimulación cognitiva. Este proceso mejora directamente la función ejecutiva, la atención y la capacidad de aprendizaje. Al definir objetivos específicos y alcanzables, se fomenta la motivación y la autoeficacia, componentes cruciales para el esfuerzo sostenido y el logro, y que se alinean directamente con el concepto de “plan vital” de la BBHI.
6.3.3 Pilar 3: El Ciudadano Comprometido—Los Dividendos Cognitivos de la Participación Comunitaria
El voluntariado y la participación en la comunidad son manifestaciones externas de un propósito interno y conllevan notables beneficios para el cerebro. Un estudio de la Universidad de California en Davis reveló que el voluntariado en la vejez está específicamente asociado con una mejor función ejecutiva y memoria episódica. De hecho, aquellos que realizaban voluntariado varias veces por semana presentaban los niveles más altos de función ejecutiva.
La potencia del voluntariado radica en que aglutina varios factores protectores en una sola actividad: ofrece estimulación cognitiva (aprender nuevas tareas y roles), fomenta la interacción social (trabajar en equipo) y a menudo implica actividad física, todo ello mientras refuerza un sentido de propósito y contribución al bien común. No es de extrañar que el estudio de Howard et al. destacara el trabajo profesional, el voluntariado y la mentoría como actividades clave que contribuyen a la salud cerebral.
6.3.4 Pilar 4: El Espíritu Resiliente—Fe, Espiritualidad y Neuroprotección
Para muchas personas, la fe y la espiritualidad son la principal fuente de propósito y significado. La investigación científica respalda el papel neuroprotector de estas prácticas. Estudios longitudinales de gran envergadura, como el “Estudio de las Monjas” y el “Estudio de las Órdenes Religiosas”, han demostrado que un mayor compromiso religioso y espiritual se asocia con un menor riesgo de desarrollar alzhéimer y un declive cognitivo más lento.
Los mecanismos propuestos son múltiples. La fe proporciona un marco robusto para encontrar sentido a la vida y afrontar la adversidad. La participación en comunidades religiosas ofrece una red social integrada y de apoyo, combatiendo directamente el aislamiento. Además, prácticas como la oración y la meditación han demostrado estimular la respuesta de relajación del cuerpo, lo que puede reducir las hormonas del estrés como el cortisol y mitigar la neuroinflamación. Finalmente, muchas actividades religiosas, como el estudio de textos o la participación en servicios, son inherentemente estimulantes desde el punto de vista cognitivo.
6.3.5 Pilar 5: Los Cimientos de la Salud—Dieta y Actividad Física
Aunque el propósito es el motor, el cuerpo es el vehículo. Una dieta saludable y el ejercicio regular son los cimientos indispensables sobre los que se construye la resiliencia cerebral.
En el ámbito de la nutrición, la dieta MIND (Mediterranean-DASH Intervention for Neurodegenerative Delay) ha surgido como el patrón dietético más específicamente diseñado para la salud cerebral. Esta dieta híbrida enfatiza el consumo de verduras de hoja verde, bayas, frutos secos, cereales integrales y pescado, mientras que limita estrictamente la carne roja, la mantequilla, el queso, los dulces y los alimentos fritos. La evidencia es sólida: una alta adherencia a la dieta MIND se asocia con un ritmo de deterioro cognitivo significativamente más lento y una reducción del riesgo de alzhéimer de hasta un 53% en algunos estudios.
En cuanto a la actividad física, la Asociación Americana del Corazón recomienda al menos 150 minutos de actividad aeróbica de intensidad moderada o 75 minutos de intensidad vigorosa por semana, complementados con ejercicios de fortalecimiento muscular dos veces por semana. La investigación específica sobre la demencia muestra que incluso cantidades modestas de ejercicio, como 35 minutos a la semana, se asocian con reducciones significativas del riesgo. Actividades cotidianas como caminar a paso ligero, la jardinería o incluso las tareas domésticas también contribuyen a la salud cerebral.
Estos cinco pilares no deben verse como elementos aislados en una lista de verificación. Forman un ecosistema profundamente interconectado y autorreforzado. El propósito vital no es simplemente un pilar más; es la piedra angular que sostiene y da coherencia a todo el arco. Como ha observado el investigador Dan Buettner, las personas con un fuerte sentido del propósito son intrínsecamente más propensas a mantenerse activas, comer bien y conectar socialmente. Una persona con un “porqué” claro (su propósito, su ikigai) adoptará de forma más natural y sostenible el “cómo” (los comportamientos saludables). Por lo tanto, el primer paso para construir una vida de resiliencia cognitiva no es prescribir comportamientos, sino ayudar a cultivar un propósito.
PilarEstrategia ClaveEvidencia de Respaldo (Estudios/Revisiones Clave)Mecanismo Neuroprotector PropuestoVínculo con el Propósito****1. Conexión SocialMantener una red social activa y relaciones de calidad.Metaanálisis de Kuiper et al.Fortalece los circuitos neuronales, amortigua el estrés.El propósito a menudo se encuentra en las relaciones.2. Compromiso MentalParticipar en el aprendizaje permanente y establecer metas.Estudio de Duke/Xu et al.; Estudio de Clare et al.Construye la reserva cognitiva, mejora la neuroplasticidad.El propósito requiere metas y planificación activa.3. Participación ComunitariaRealizar voluntariado o mentoría de forma regular.Estudio de UC Davis/Lor et al.Combina estimulación social, cognitiva y física.El propósito se expresa a menudo a través del servicio.4. Bienestar EspiritualPracticar la fe, la espiritualidad o la meditación.Estudio de las Órdenes ReligiosasReduce las hormonas del estrés, proporciona apoyo social.El propósito proporciona significado y resiliencia.5. Salud FundamentalAdherirse a la dieta MIND y a las pautas de ejercicio.Estudio de Morris et al. (MIND); AHA Recs.Reduce la neuroinflamación y el estrés oxidativo.El propósito motiva los comportamientos saludables.
6.4 Una Nueva Frontera en el Manejo del Alzhéimer: Estilo de Vida vs. Fármacos
La llegada de los primeros fármacos que modifican el curso de la enfermedad de Alzheimer ha generado un gran entusiasmo, pero también ha puesto de relieve las profundas diferencias entre un enfoque de tratamiento y un enfoque de prevención.
6.4.1 El Advenimiento de las Terapias Anti-Amiloides
Los anticuerpos monoclonales diseñados para unirse y eliminar las placas de beta-amiloide del cerebro, una de las principales características patológicas de la enfermedad, son un hito en la investigación de la enfermedad.
Su eficacia clínica, aunque estadísticamente significativa, ha sido descrita como modesta. No cura ni revierte la enfermedad, pero ha demostrado ralentizar la tasa de deterioro cognitivo en pacientes que se encuentran en las etapas iniciales de la enfermedad de Alzheimer (deterioro cognitivo leve o demencia leve).
Sin embargo, este modesto beneficio viene acompañado de importantes preocupaciones de seguridad. El efecto secundario más notable son las Anomalías de Imagen Relacionadas con el Amiloide (ARIA), el riesgo de ARIA es particularmente elevado en personas que son portadoras de dos copias del alelo APOE-e4, lo que hace necesario realizar pruebas genéticas antes de iniciar el tratamiento. A esto se suman los elevados costes del fármaco y la necesidad de una monitorización intensiva con resonancias magnéticas periódicas, lo que plantea barreras significativas de acceso y equidad.
6.4.2 Una Estrategia Integrada para la Salud Pública: Una Encrucijada Crítica
La aparición de estos fármacos sitúan a la sociedad y a los sistemas sanitarios en una encrucijada crítica. Existe el riesgo de que el atractivo de una “bala de plata” farmacéutica desvíe la atención y los recursos del trabajo, menos glamuroso pero potencialmente más impactante, de la prevención primaria a través del estilo de vida.
La comparación directa entre ambos enfoques es reveladora. Por un lado, tenemos una intervención farmacéutica de alta tecnología, alto coste y alto riesgo, dirigida a un grupo selecto de pacientes que ya han comenzado a desarrollar la enfermedad. Por otro lado, una intervención de estilo de vida sin coste, sin riesgo y universalmente accesible, centrada en prevenir que la enfermedad se manifieste en primer lugar.
Estos enfoques no son mutuamente excluyentes, sino complementarios. Las innovaciones farmacéuticas son vitales para tratar la enfermedad existente. Sin embargo, las intervenciones de estilo de vida, con el propósito como eje central, son la herramienta más poderosa para prevenirla. Una política de salud pública eficaz no puede centrarse únicamente en tratamientos costosos para unos pocos; debe invertir masivamente en la promoción de estrategias preventivas, escalables y equitativas para la mayoría. La verdadera forma de “perderle el miedo al alzhéimer” no reside solo en ofrecer un tratamiento arriesgado al 1% que desarrolla la enfermedad, sino en empoderar al 99% para que reduzca su riesgo de necesitarlo alguna vez.
MétricaEstilo de Vida con PropósitoAnticuerpos monoclonales****Población ObjetivoPoblación general (prevención primaria).Pacientes en fase inicial de EA (tratamiento).EficaciaReducción del riesgo de ~28%; retraso de 1.4 meses en la aparición.Ralentización modesta de la progresión.Mecanismo PrincipalMejora de la reserva cognitiva y la neuro-resiliencia.Eliminación de placas de amiloide.Seguridad/Efectos SecundariosNinguno; efectos positivos en la salud general.ARIA (edema/hemorragia cerebral), reacciones a la infusión.CosteGratuito.Costes farmacéuticos y de monitorización elevados.AccesibilidadUniversalmente accesible.Requiere atención especializada, RMNs, pruebas genéticas.
La enfermedad de Alzheimer persiste como uno de los mayores desafíos para la salud pública del siglo XXI. Sin embargo, la investigación científica está reescribiendo la narrativa de esta enfermedad, transitando de una de fatalismo ineludible a una de empoderamiento y agencia. La evidencia es cada vez más clara: aunque no podemos modificar nuestros genes ni detener el paso del tiempo, una parte sustancial del riesgo de desarrollar demencia es modificable. El estudio de Howard, Wingo y sus colaboradores ha proporcionado una prueba cuantitativa de lo que las comunidades longevas como la de Loma Linda han sabido intuitivamente durante generaciones: una vida con un fuerte sentido de propósito es una vida más sana y resiliente. Este efecto protector no es una mera correlación conductual; la evidencia neurobiológica emergente sugiere que el propósito puede esculpir activamente la estructura y función de nuestro cerebro, construyendo una reserva que nos defiende contra el asedio de la patología. Los cinco pilares de la longevidad cognitiva no son prescripciones aisladas, sino las manifestaciones de una vida vivida con intención. El secreto de los supercentenarios no reside en un suplemento exótico o una anomalía genética, sino en una lección profundamente humana sobre el valor del significado y la conexión. La prevención de la enfermedad de Alzheimer, por tanto, no comienza en la farmacia, sino en nuestras comunidades, en nuestras relaciones y en la búsqueda diaria de nuestro propio “ikigai”. Cada uno de nosotros tiene la capacidad de ser el autor de una vida que no solo sea más larga, sino cognitivamente más vibrante y, en última instancia, más significativa.
Conclusión Final: La Profecía del Escultor
El análisis de la obra de Santiago Ramón y Cajal revela que fue el arquitecto invisible de nuestra comprensión de la enfermedad de Alzheimer. Mientras que Alois Alzheimer dio a la enfermedad un nombre y un rostro, Cajal proporcionó la gramática biológica que nos permitió leer su devastadora historia. Su Doctrina de la Neurona creó el propio objeto de estudio: la célula individual que enferma y muere. Sus estudios sobre la degeneración y la regeneración describieron la trágica dinámica de la lucha de esa célula por sobrevivir en un entorno hostil, un proceso que se desarrolla de forma dramática alrededor de las placas seniles. Sus hipótesis sobre los factores de crecimiento y guía química sentaron las bases para las terapias regenerativas modernas.
El artículo concluye con la célebre y conmovedora cita de Cajal, pronunciada en la época en que recibió el Premio Nobel, que durante más de un siglo resonó como un dogma:
“Los circuitos nerviosos son algo fijo, cerrado e inmutable. Todo puede morir, pero nada puede regenerarse. Es tarea de la ciencia del futuro modificar este cruel decreto.”
El eco de sus palabras resuena hoy con una fuerza renovada, ya que esa “ciencia del futuro” ha llegado, y lo ha hecho, poéticamente, en el instituto del CSIC que lleva su nombre. Por ejemplo, Investigaciones recientes lideradas por la neurobióloga Aixa V. Morales en el Instituto Cajal han descubierto un mecanismo capaz de reactivar las células madre del cerebro adulto en ratones para generar nuevas neuronas. Este avance en neurogénesis, que busca precisamente “modificar el cruel decreto”, abre vías esperanzadoras para intervenir en la pérdida de capacidad cognitiva que provocan enfermedades como el alzhéimer. El desafío de Cajal sigue siendo la misión central que anima la investigación actual, convirtiendo a los científicos contemporáneos en los herederos intelectuales directos de su visión profética.
Referencias Bibliográficas
-
Ramón y Cajal, S. (1909-1911). Histologie du système nerveux de l’homme & des vertébrés. Maloine.
-
Ramón y Cajal, S. (1913-1914). Estudios sobre la degeneración y regeneración del sistema nervioso. Hijos de Nicolás Moya.
-
García-Marín, V., García-López, P., & Freire, M. (2007). Cajal’s contributions to the study of Alzheimer’s disease. Journal of Alzheimer’s Disease, 12(2), 161-174.
-
Oscar, L. C. (2014). Nicolás Achúcarro (1880-1918). Neurosciences and History, 2(2), 74-78.
-
Sierra, A., de Castro, F., Del Río-Hortega, J., Rafael-Nadal, R. A., & Valles, S. L. (2016). The “Big-Bang” of modern glial biology: Translation and comments on Pío del Río-Hortega’s seminal article on microglia. Glia, 64(11), 1801-1840.
-
Mateos-Aparicio, P., & Rodríguez-Moreno, A. (2019). The impact of studying brain plasticity. Frontiers in Cellular Neuroscience, 13, 66.
-
Livingston, G., Huntley, J., Sommerlad, A., Ames, D., Ballard, C., Banerjee, S.,… & Mukadam, N. (2020). Dementia prevention, intervention, and care: 2020 report of the Lancet Commission. The Lancet, 396(10248), 413-446.
-
Howard, N. C., Wingo, A. P., Thambisetty, M., & Wingo, T. S. (2025). Purpose in Life and Risk of Cognitive Impairment. The American Journal of Geriatric Psychiatry.




Comentarios