Un Reconocimiento a la Vanguardia Científica
En el solemne discurrir de sus más de ocho siglos de historia, la Universidad de Salamanca ha sido faro del saber y testigo de las grandes revoluciones del pensamiento. Fiel a esa herencia, la institución se prepara para un acto que une su venerable tradición con la vanguardia más disruptiva de la ciencia contemporánea. El próximo 24 de octubre, el Claustro de Doctores investirá a la Dra. Emmanuelle Charpentier, laureada con el Premio Nobel, con el título de Doctora Honoris Causa, la máxima distinción que emana de su seno académico. Esta ceremonia trasciende el homenaje a una carrera excepcional; es un acto de profunda significación que celebra el poder de la curiosidad humana y el compromiso de la Universidad con la ciencia que está redefiniendo el porvenir de la humanidad.
La propuesta para este honor, un gesto de inmenso calado intelectual, partió de una entidad cuya misión encarna la esperanza en la lucha contra la enfermedad: el Centro de Investigación del Cáncer (CIC), un instituto de excelencia forjado en la sinergia de la USAL y el CSIC. La defensa de la candidatura, a cargo del profesor Alberto Martín Pendás, revela una conexión que no es casual, sino causal. Honrar a Charpentier es un reconocimiento a la creadora de una herramienta que ha supuesto un antes y un después en la biología molecular, una herramienta que los propios investigadores del CIC emplean en su quehacer diario. La justificación de la USAL resuena con esta verdad, destacando la “trascendencia del trabajo de Charpentier” y su poder para abrir “innumerables posibilidades… de manera particular, en la investigación oncológica”. El acto es, por tanto, el encuentro simbólico entre la arquitecta de la revolución genómica y los artífices que, con sus herramientas, construyen cada día el futuro de la medicina.
Emmanuelle Charpentier, microbióloga, genetista y bioquímica francesa, recibió junto a su colaboradora Jennifer A. Doudna el Premio Nobel de Química en 2020 “por el desarrollo de un método para la edición del genoma”. El galardón llegó apenas ocho años después de la publicación de su trabajo seminal en 2012, un hecho que la propia Charpentier ha calificado de inusual, pues la Academia sueca suele esperar décadas para consagrar un descubrimiento. Esta vertiginosa cadencia de reconocimientos —desde el Premio Princesa de Asturias en 2015 hasta el Nobel y ahora el Doctorado Honoris Causa— narra la crónica de una tecnología cuyo impacto fue tan inmediato, tan innegable y tan profundo, que la comunidad científica global no tuvo más remedio que rendirse a su evidencia.
La Arquitecta de la Revolución Genética: El Viaje Científico de Emmanuelle Charpentier
La trayectoria de Emmanuelle Charpentier es un elocuente testimonio de una verdad que a menudo se olvida: las más grandes innovaciones tecnológicas germinan en el fértil terreno de la ciencia fundamental, aquella impulsada no por la aplicación, sino por el puro anhelo de comprender. Nacida en Juvisy-sur-Orge, Francia, el 11 de diciembre de 1968, su formación culminó con un Doctorado en Microbiología en el prestigioso Instituto Pasteur. Desde sus inicios, su carrera se ha consagrado a desentrañar los “mecanismos fundamentales de las enfermedades”, con un foco preciso en las bacterias patógenas como Streptococcus pyogenes.
Su camino hacia CRISPR-Cas9 no comenzó con la meta de inventar una herramienta, sino con una pregunta esencial: ¿cómo regulan sus genes las bacterias para causar enfermedades?. Fue esta inmersión profunda en el universo de las pequeñas moléculas de ARN reguladoras en S. pyogenes lo que la condujo, como un navegante que descubre un nuevo continente buscando una ruta conocida, al sistema CRISPR. En sus propias palabras, resuena el eco de la ciencia movida por la curiosidad: “Fue así, centrándome en estas moléculas de ARN, como llegué a CRISPR”. Como ella misma ha afirmado con la rotundidad de un principio epistemológico, todas las grandes herramientas de la biotecnología “tienen su origen en la investigación fundamental sobre las bacterias y los virus”. Su trabajo es, por tanto, un poderoso alegato en favor de la investigación básica, demostrando que los avances más transformadores a menudo provienen de las fuentes más inesperadas. “Sin la ciencia básica”, sentencia, “sin la comprensión de los mecanismos que las bacterias han desarrollado para defenderse […], no habría surgido esta tecnología”.
La elección de Streptococcus pyogenes fue providencial. Este patógeno alberga un sistema CRISPR-Cas de Clase 2, Tipo II, de una simplicidad asombrosa en comparación con otros sistemas inmunitarios bacterianos. Mientras otros sistemas requieren un complejo de múltiples proteínas, el de S. pyogenes depende de una única y versátil proteína: la Cas9. La profunda especialización de Charpentier en la biología de esta bacteria le otorgó una atalaya privilegiada para descifrar este mecanismo elegante y minimalista. Su viaje demuestra cómo la inmersión rigurosa en un campo específico del saber puede desencadenar consecuencias de un alcance universal inimaginable.
Hoy, como Directora Fundadora de la Unidad Max Planck para la Ciencia de los Patógenos en Berlín y cofundadora de CRISPR Therapeutics, Charpentier sigue en la vanguardia del conocimiento que ella misma ayudó a crear. Su carrera está jalonada por los más altos honores, desde el Premio Fundación BBVA Fronteras del Conocimiento (2016) hasta el Premio Wolf de Medicina (2020) y la cúspide del Nobel. Cada premio es un hito en la cronología de una revolución que sigue en marcha, una revolución nacida de la simple y profunda pregunta de cómo funciona la vida.
De la Inmunidad Bacteriana a una Herramienta Universal: La Historia de CRISPR-Cas9
La génesis de CRISPR-Cas9 es una saga científica que aúna la observación minuciosa, la colaboración internacional y un instante de genialidad ingenieril. En su esencia, el sistema CRISPR es un antiquísimo y sofisticado mecanismo de defensa, un sistema inmunitario adaptativo que las bacterias han perfeccionado durante eones para protegerse de la incesante amenaza de los virus.
Un Archivo Genético de Infecciones Pasadas
Durante años, los científicos observaron en los genomas bacterianos unas extrañas secuencias repetitivas, a las que bautizaron como CRISPR (Repeticiones Palindrómicas Cortas Agrupadas y Regularmente Interespaciadas). El gran descubrimiento fue constatar que las secuencias únicas intercaladas entre dichas repeticiones, los “espaciadores”, eran fragmentos de ADN de virus que habían atacado a la bacteria en el pasado. El locus CRISPR funciona, por tanto, como una biblioteca genética, una “memoria de ‘agresiones genéticas’ pasadas” que permite a la bacteria reconocer y aniquilar a futuros invasores. Junto a este archivo se encuentran los genes cas, que codifican las proteínas ejecutoras, siendo la Cas9 la “tijera” molecular que corta el ADN viral.
El Descubrimiento Clave: La Molécula Ignorada
El punto de inflexión en esta historia se produjo en 2011 en el laboratorio de Emmanuelle Charpentier. Su equipo, mientras cartografiaba el universo de pequeños ARNs en S. pyogenes, identificó una molécula abundante y hasta entonces desconocida, a la que llamaron tracrRNA (ARN de CRISPR trans-activador).
Este hallazgo fue la piedra de Rosetta que permitió descifrar el sistema. Charpentier demostró que el tracrRNA tenía una doble función, ambas cruciales. Primero, se aparea con el ARN precursor de CRISPR, formando una estructura que es procesada por una enzima de la bacteria (RNasa III) para generar los ARN guía maduros (crRNA). Segundo, y aún más decisivo, el mismo tracrRNA es indispensable para activar la proteína Cas9, permitiéndole reconocer y cortar su ADN diana. El tracrRNA era el manual de instrucciones que la comunidad científica había estado buscando. Este descubrimiento transformó a CRISPR de una curiosidad microbiológica a una herramienta con un potencial prometeico.
Una Colaboración “Corta e Intensa” y el Salto a la Bioingeniería
Consciente de la magnitud de su hallazgo, Charpentier se acercó a Jennifer Doudna, una reconocida experta en la estructura del ARN, durante una conferencia científica. Juntas, en una serie de elegantes experimentos in vitro, demostraron que la proteína Cas9, guiada por el complejo de los dos ARNs (crRNA y tracrRNA), podía ser programada para cortar cualquier molécula de ADN en una secuencia específica. La colaboración, que Charpentier describe como “corta e intensa”, estuvo impulsada por la certeza compartida de que “la historia era magnífica” y que “necesitaban ir rápido” para desvelarla al mundo.
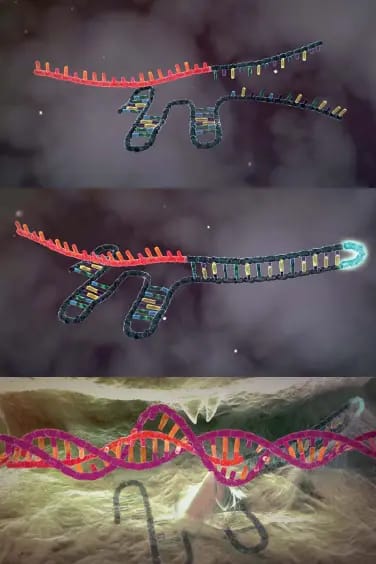
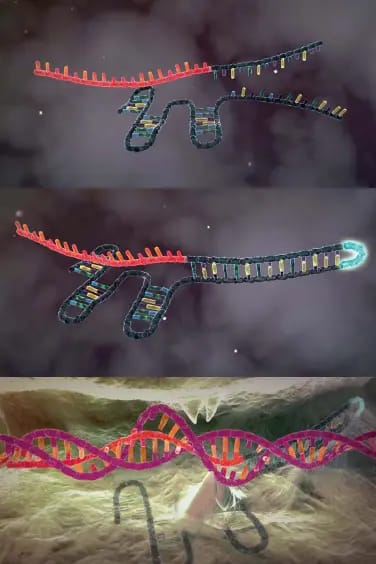
El golpe de genio final, el que transmutó un descubrimiento en una revolución, fue un acto de bioingeniería. Se dieron cuenta de que las dos moléculas de ARN podían fusionarse en una sola molécula quimérica: el ARN de guía única (sgRNA). Este diseño magistral simplificó el sistema de forma radical, reduciéndolo a una herramienta de dos componentes de una sencillez pasmosa: la proteína Cas9 y un sgRNA programable. En su artículo de 2012 en Science, concluyeron con clarividencia que su estudio revelaba el “potencial de explotar el sistema para la edición del genoma programable por ARN”. Este salto conceptual, de la observación de la naturaleza a su rediseño racional, fue la chispa que encendió la revolución CRISPR.
Reescribiendo el Código de la Vida: El Impacto Biomédico y en la Investigación
La invención de la herramienta CRISPR-Cas9 ha catalizado una transformación sin parangón en las ciencias de la vida. Su poder no radica solo en su precisión, sino en su asombrosa simplicidad y accesibilidad, lo que ha permitido una “explosión de conocimiento” y su adopción masiva en laboratorios de todo el mundo.
El Mecanismo de Edición Genómica
Para editar el genoma, los científicos introducen en una célula la proteína Cas9 y un sgRNA diseñado para coincidir con un lugar específico del ADN. El sgRNA actúa como un lazarillo molecular, guiando a la Cas9 hasta su diana. Allí, la proteína ejecuta un corte limpio en la doble hélice del ADN. A partir de este punto, los sistemas naturales de reparación de la propia célula toman el relevo.
La célula puede reparar el corte por dos vías principales. Una, rápida pero propensa a errores (NHEJ), suele inactivar el gen, lo que permite a los científicos estudiar su función. La otra, más precisa (HDR), puede utilizar una plantilla de ADN proporcionada por el investigador para reparar el corte, permitiendo corregir mutaciones que causan enfermedades o insertar nuevas secuencias genéticas con una precisión exquisita.
Una Fuerza Democratizadora en la Ciencia
Antes de CRISPR, las tecnologías de edición genética eran complejas y costosas, un arcano reservado a unos pocos laboratorios de élite. La llegada de CRISPR-Cas9, una herramienta “sencilla, fácil de usar y barata”, cambió el paradigma. Ha “revolucionado absolutamente la biología”, permitiendo a los investigadores responder preguntas de forma “mucho más rápida, eficiente y económica”. Se ha convertido en una pieza fundamental de la “caja de herramientas” de cualquier biólogo molecular. Este acceso democratizado ha acelerado el ritmo del descubrimiento a una escala global, empoderando a una nueva generación de científicos.
Aplicaciones Terapéuticas y Relevancia Oncológica
El potencial terapéutico de CRISPR es inmenso. Ya existen ensayos clínicos avanzados que utilizan esta tecnología para tratar enfermedades de la sangre como la anemia falciforme y la β-talasemia, con resultados esperanzadores.
En el campo de la oncología, de particular relevancia para el Centro de Investigación del Cáncer de Salamanca, el impacto es igualmente profundo. La tecnología se utiliza de forma rutinaria para crear modelos de la enfermedad y probar nuevas terapias. Una de las aplicaciones más prometedoras es la inmunoterapia, en la generación de las llamadas células CAR-T. Mediante CRISPR, se pueden modificar los linfocitos T de un paciente para que reconozcan y destruyan selectivamente las células tumorales.
El descubrimiento de Charpentier no es una invención estática, sino una plataforma para la innovación continua. Ya han surgido herramientas derivadas, como los “editores de bases” o los “editores primarios”, que permiten cambiar letras individuales del código genético con una precisión aún mayor. Charpentier visualiza un futuro en el que la tecnología evolucione de un modelo de “prêt-à-porter a la alta costura”, con sistemas de edición diseñados a medida para aplicaciones específicas.
El Futuro es Ahora: Conciencia y Responsabilidad ante una Tecnología Transformadora
La capacidad de reescribir el código de la vida ha abierto un horizonte de posibilidades sin precedentes, pero también ha planteado profundos interrogantes éticos que exigen una reflexión serena y un diálogo global.
La Visión de la Científica y los Desafíos Futuros
Desde la perspectiva de Emmanuelle Charpentier, el futuro de la tecnología pasa por perfeccionar su precisión y, sobre todo, por resolver el desafío de su entrega (delivery): cómo hacer llegar el sistema CRISPR-Cas9 a las células correctas dentro del cuerpo humano de forma segura y eficiente.
Ética, Regulación y el Científico como Gestor Público
El poder de esta tecnología plantea “serios problemas éticos y sociales” que deben ser abordados con la máxima responsabilidad. El debate se ha centrado en la edición de la línea germinal humana —la modificación de óvulos, espermatozoides o embriones—, ya que estos cambios serían hereditarios.
En esta conversación crucial, tanto Charpentier como Doudna han asumido un papel de liderazgo ejemplar. Lejos de encerrarse en su laboratorio, han participado activamente en el debate público, abogando por la necesidad de una regulación meditada y la participación de toda la sociedad. Este modelo de científico como custodio público de su propio descubrimiento establece un nuevo estándar de responsabilidad para la ciencia del siglo XXI. Charpentier insiste en la importancia de que la ciencia no pierda su “sentido de la profundidad y la ética” en la carrera por las aplicaciones.
La concesión del Premio Nobel a dos mujeres, por primera vez en la historia de los premios de ciencias sin un co-laureado masculino, es en sí misma un hito. Charpentier ha expresado que esto envía un “mensaje muy positivo a las niñas y jóvenes interesadas en la ciencia”, demostrando que los máximos reconocimientos son alcanzables. Su visita a la Universidad de Salamanca es, por tanto, una oportunidad no solo para celebrar la ciencia, sino para inspirar a la próxima generación de investigadores e investigadoras que se forman en sus aulas.
Una Invitación a un Evento Histórico
La visita de la Dra. Emmanuelle Charpentier a la Universidad de Salamanca constituye una oportunidad única para toda la comunidad universitaria y para la sociedad en su conjunto. Es una ocasión para escuchar directamente a una de las mentes científicas más influyentes de nuestro tiempo, una investigadora cuyo trabajo no solo ha merecido el Premio Nobel, sino que ha redefinido las fronteras de lo posible.
Se invita a estudiantes, investigadores, profesores y al público interesado a asistir a los actos programados. Serán testigos no solo de la concesión de la más alta distinción académica de esta Universidad a una figura monumental, sino de la celebración del conocimiento, la perseverancia y el poder de la ciencia para transformar el mundo.
Tabla 1: Agenda de Actos: Dra. Emmanuelle Charpentier en la Universidad de Salamanca
ActoFechaHora****LugarSeminario Científico23 de octubre12:30hSalón de actos DioscóridesCeremonia de Investidura Doctora Honoris Causa24 de octubre12hParaninfo de la Universidad
Investidura como Doctora Honoris Causa
Emmanuelle Charpentier - Chemistry Prize 2020Descarga
Imagen de portada: Emmanuelle Charpentier foto de © Hallbauer and Fioretti



Comentarios